Навигация
Моль аммиака образуют 12 моль воды
8 моль аммиака образуют 12 моль воды
314,23 кмоль аммиака образуют х кмоль воды
Х3 = 471,34 кмоль\час
Определяем количество водяных паров, образовавшихся после окисления аммиака:
С(Н2О)общ. = х1 + х3 (2.7)
С(Н2О)общ. = 5,57 + 471,34 = 476,91 кмоль\час
Количество расходуемого кислорода на окисление аммиака до оксидов азота по реакции (2) в час:
4 моль аммиака требуют 5 моль кислорода
314,23 кмоль аммиака требуют х кмоль кислорода.
Х4 = 392,78 кмоль \ час кислорода.
Количество расходуемого кислорода на окисление аммиака до оксида азота по реакции (3) принимаем 4 % от общего кислорода.
С(О2 – N2) = 0.75 * С1NH3 (1 – ŋК) (2.8)
С(О2 – N2) = 0,75 * 5342,08 * 0,025 = 3,13 кмоль \ час
Общий расход кислорода составит:
С(О2)общ = х4 + С(О2 – N2) (2,9)
С(О2)общ = 392,78 + 3,13 = 395,91 кмоль \ час
Определяем, сколько остается кислорода в газовой смеси после окисления аммиака:
СОСТ. = С1 О2 - С(О2)общ (2.10)
СОСТ. = 574,67 – 395,91 = 178,76 кмоль \ час
Таблица 8 – Расход из контактного аппарата
| Компонент | Кмоль | % об. | Кг | % вес. |
| Аммиак | 304,803 | 9,74 | 9144,09 | 10,87 |
| Кислород | 178,76 | 5,71 | 5720,32 | 6,80 |
| Азот | 2166,57 | 69,28 | 60663,96 | 72,12 |
| Вода | 476,91 | 15,25 | 8584,38 | 10,21 |
| Итого: | 3127,043 | 100 | 84112,75 | 100 |
Похожие работы
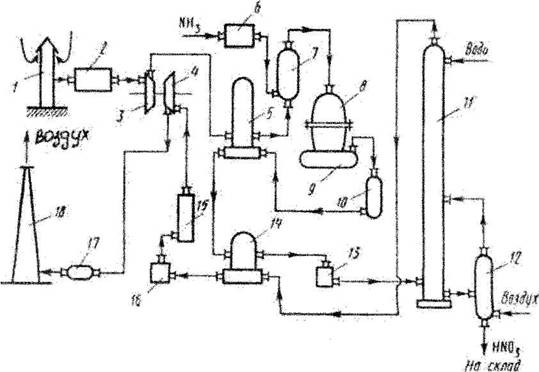
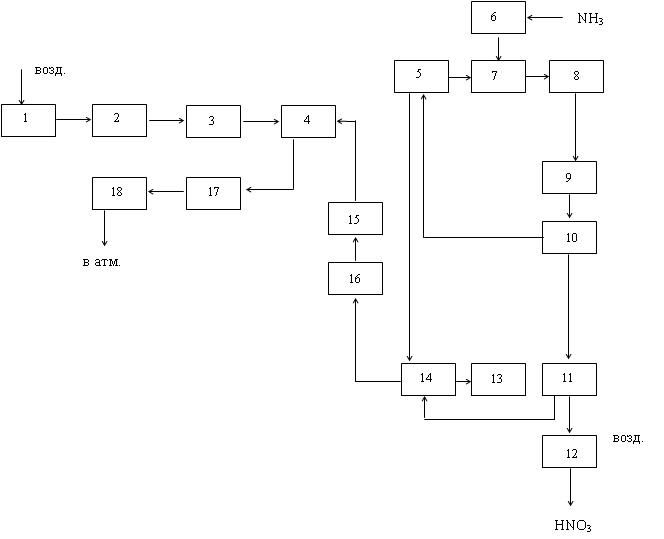
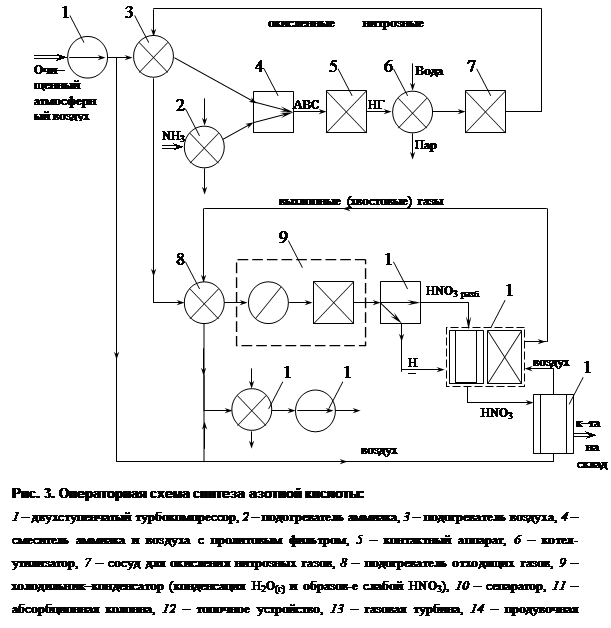
... + 50 2 = 4NO + 6Н2О 2NO+O2=2NO2 3NO2 + H2O = 2NО3 + N0 NH3 + 2О2 = HNO3 + Н2О + 421,2 Технологическая схема Рис. 3. Технологическая схема производства азотной кислоты 1-воздухозаборная труба; 2-воздухоочиститель; 3-газовый компрессор; 4-газовая турбина; 5-воздухоподогреватель; 6-испаритель аммиака; 7-смеситель с фильтром; 8-контактный аппарат; 9,17-котёл-утилизатор; 10-окислитель с ...
... в производстве концентрированной азотной кислоты по методу прямого синтеза. В отдельных случаях используется для обогащения АВС при получении неконцентрированной азотной кислоты. СОВРЕМЕННОЕ СОСТОЯНИЕ ТЕХНОЛОГИИ ПРОИЗВОДСТВА НЕКОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ. Азотная кислота и главным образом ее природная соль - натриевая селитра известны с давних времен. В 778 г. Арабский ученый Гебер ...
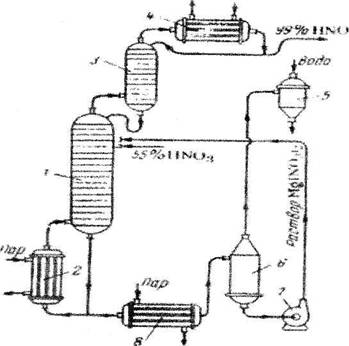
... очистки выхлопных газов, выпускающий продукцию в виде 53–58% -ной HNO3. Технологическая схема этого производства в упрощенном варианте представлена на рисунке 5. Подготовка сырья Рис.5 Схема производства азотной кислоты под давлением 0,716 МПа с приводом компрессора от газовой турбины: 1 – фильтр воздуха; 2 – реактор каталитической очистки; 3 – топочное устройство; 4 – ...
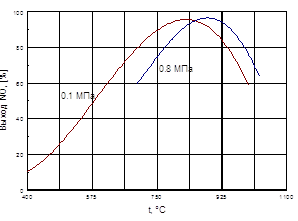
... способствует образованию NO2. При температурах до 100 ºС равновесие реакции практически полностью сдвинуто в правую сторону. Окисление диоксида азота – самая медленная стадия получения азотной кислоты. Она сильно зависит от концентрации реагентов, давления температуры. Применение воздуха, обогащенного кислородом (или чистого кислорода) позволяет получать НГ[2] с повышенным содержанием ...




0 комментариев