Навигация
Тепловой расчет
2.3 Тепловой расчет
Определяем приход тепла по реакциям
4NH3 + 5O2 = 4NO + 6H2O + 908 кДж (4)
4NH3 + 3О2 = 2NO3 + 6H2O + 1270кДж (5)
Q1 = QP * ПЧАС \ 4 * 10613, 3 (3.1)
Где QP – тепло в реакции,
ПЧАС – производительность часовая,
4 – коэффициент по реакции.
Q1 = 908 * 22,47 \ 4 * 10613,3 = 54135153 кДж = 5,4 * 107 кДж
Q2 = 1270 * 22,47 \ 2 * 219 = 3124790,6 кДж = 3,1 * 106 кДж
Определяем приход тепла с аммиачно-воздушной смесью, поступающей в контактный аппарат.
Q3 = m * c * tX (3.2)
Где: m – количество поступающей аммиачно-воздушной смеси, кмоль,
с – средние мольные теплоемкости компонентов смеси в пределах от 0 до 250 ˚С, они составляют:
38,5 Дж для аммиака,
30,2 Дж для кислорода,
29,2 Дж для азота.
tX – температура смеси, ˚С.
Q3 = (38,5 * 314,23 + 30,2 * 574,67 + 29,2 * 2161,86) tX = 9,2 * 104 tX кДж
Определяем расход тепла с уходящими от сеток нитрозными газами при температуре конверсии 900 ˚С.
Q4 = (31,9 * 304,803 + 32,6 * 178,76 + 29,2 * 2166,57) * 900 = 7,09 * 107 кДж
Потери тепла за счет изменения тепла, вызывающих понижение температуры катализаторных сеток, составляет:
Q5 = 0, 05 * Q4 (3.3)
Q5 = 0,05 * 7,09 * 107 = 3,54 * 106 кДж
Исходя из количества поступающего и расходуемого тепла можно определить температуру tX аммиачно-воздушной смеси, поступающей в конвертор.
Q = Q1 + Q2 + Q3 + Q4 + Q5 (3.4)
Где Q1 – приход тепла по реакции (4),
Q2 – приход тепла по реакции (5),
Q3 – приход тепла с аммиачно-воздушной смесью, поступающей в контактный аппарат,
Q4 – расход тепла с уходящими от сеток газами,
Q5 – потери тепла за счет изменения тепла, вызывающих понижение температуры катализаторных сеток.
Q = 5,4 * 107 + 3,1 * 106 + 9,2 * 104 + 7,09 * 107 + 3,54 * 106 = 13179,17 * 104 = 1,3 * 108 кДж
tX = Q + q \ mНГ * сНГ (3.5)
где: q – тепло с аммиачно-воздушной смесью,
mНГ – количество нитрозных газов,
сНГ – средняя теплоемкость нитрозных газов (1,223 кДж \ кг * град)
tX = 1,3 * 108 + 9,2 * 104 \ 84112,75 * 1,223 = 128,2 ˚С.
Котел-утилизатор
В данном случае тепло газа расходуется на получение пара, поэтому уравнение теплового баланса имеет вид:
Q = (W – W0) *св * (t2K – t2H) + W0 (J – св * t2H ) (3.6)
Где W – количество подаваемой на орошение воды, кг \ с;
Св – удельная теплоемкость воды, Дж \ кг ˚С;
t2K – конечная температура питательной воды, ˚С;
t2H – начальная температура питательной воды, ˚С;
W0 – количество испарившейся воды, кг \ с.
W0 = В * F0 (x “ – x) (3.7)
Где В – коэффициент испарения, кг \ м2 к;
F0 – площадь испарения, м2;
x “ – влагосодержание пара в месте соприкосновения его с водой;
х – влагосодержание пара в газообразном объеме, кг.
Площадь испарения определяем из уравнения:
F = 2 * 420 = 840 м2
W0 = 200 *840 (0,89 – 0,76) = 21840 кг \ ч = 6,06 кг \ с
Q = (6,9 – 6,06) 4190 (247 – 140) + 6,06 (694300 – 4190 * 140) = 276064,8 Вт
То есть для испарения 6,06 кг воды за 1 секунду требуется от нитрозного газа отнять количество теплоты в размере 276064,8 Вт.
2.4 Конструктивный расчет
2.4.1 Контактный аппарат
Время конверсии τ при температуре окисления аммиака 900 ˚С можно определить по уравнению
Lg = - 107 * k1 + 7.02 * 10-6 * k3 (4.1)
Где k1 = 0,97 – степень конверсии аммиака;
Lg = - 107 * 97 + 7,02 – 10-6 * 973 = 1,06 * 10-4 сек
Площадь сечения конвертора будет равна
S=100*τ*V0*TK*PH\1,1* m * d * PK * 273 (1 – 1.57 * den) (4.2)
Где: τ – время конверсии, сек;
V0 – объем аммиачно-воздушой смеси при 0 ˚С;
TK – температура конверсии, 900 + 273 = 1197 К;
PH – начальное давление, 9,8 * 104 н \ м3;
m – количество сеток;
d – диаметр проволоки сеток, 0,009 мм;
PK – давление газа при конверсии, 73 * 104 н\м;
n – число плетений на 1 см2, 1024 штук.
V0 = m * V \ 360 (4.3)
Где: m – масса аммиачно-воздушной смеси, кг;
V – объем при нормальных условиях.
V0 = 84112,75 * 22,4 / 360 = 5233,68 кг \ час
S = 100 * 1,06 * 10-4 * 5233,68 * 1173 * 980 \ 1,1 * 18 * 0,09 * 73 * 273 (1* * 1,57 * 0,009 * e1024) = 3,31 м 2
2.4.2 Котел-утилизатор
Сечение трубчатки
S1 = p \ 4 * dВ2 * n (4.4)
Где: dВ – внутренний диаметр трубок, м;
n – количество трубок, шт.
S1 = 3,14 \ 4 * 0,0512 * 480 = 0,98 м2
Сечение межтрубного пространства
S2 = 3,93 * S1 (4.5)
Где: 3,93 – отношение межтрубного сечения к сечению трубчатки.
S2 = 3,93 * 0,98 = 3,8 м2
Сечение, занято стенками трубок.
S3 = p \ 4 * (dH2 - dВ2) * n (4.6)
Где: dH – наружный диаметр трубок.
S3 = 3,14 \ 4 * (0,0572 – 0,0512) * 480 = 0,24 м2
Сечение кожуха трубчатки по внутреннему диаметру.
S4 = S1 + S2 + S3 (4.7)
Где: S1 – сечение трубчатки, м;
S2 – сечение межтрубного пространства, м;
S3 – сечение, занятое стенками трубок, м.
S4 = 0,98 + 3,8 + 0,24 = 5,02 м2
Определяем диаметр кожуха
D = e(4 * S4 \p) (4.8)
D = e(4 * 5.02 \ 3.14) = 2.5 м
Приведенный диаметр трубчатки определяем по уравнению
DПР = 4 * S1 \ П (4.9)
Где: П – смоченный периметр, м.
DПР = 4 * 0,98 \ 76,8 = 0,05
Смоченный периметр определяем по уравнению:
П = p * dВ * n (4.10)
П = 3,14 * 0,051 * 480 = 76,8
Определяем длину трубок
L = F \ p * dH * n * z (4.11)
Где: F – площадь теплообменника, м2;
Z – число ходов.
L = 840 \ 3.14 * 0.057 * 480 * 2 = 4,8 м = 4800 мм
Принимаем стандартную длину трубок 6000 мм.
Определяем диаметр штуцеров для подачи питательной воды.
Скорость воды принимаем равную 1 м \ сек.
dW1 = e(4 * G \ p * W2 * r) (4.12)
Где: G – расход воды, кг \ сек;
W – скорость движения питательной воды в штуцере, м \ сек;
r - плотность питательной воды.
dW1 = e(4 * 36,9 \ 3,14 * 12 * 1000) = 0,093 м или 93 мм
Принимаем стандартное значение равное 100 мм.
Определяем диаметр штуцера для отвода пара. Скорость пара в штуцерах принимаем равным 10 м \ сек.
dW2 = e(4 * G \ p * W2 * r) (4.13)
dW2 = e(4 * 6,9 \ 3,14 * 102 * 1000) = 359 мм
Принимаем стандартное значение, равное 450 мм.
Определяем диаметр штуцера для ввода нитрозных газов
dW3 = e(4 * G \ p * W2) (4.14)
dW3 = e(4 * 23.3 \ 82 * 1.4 * 3.14) = 589 мм
Диаметр штуцера для отвода нитрозных газов следует принять равным диаметру входного штуцера, то есть 600 мм, так как количество нитрозного газа, входящего в котел-утилизатор, равно количеству нитрозного газа, выходящего из него.
2.5 Расчет расходных коэффициентов
Определяем расчетный коэффициент по аммиаку на 1000 кг моногидрата азотной кислоты.
G(NH3) \ G(HNO3) (5.1)
Где: G(NH3) – количество аммиака, поступающего с аммиачно-воздушной смесью, кг \ час;
G(HNO3) – нагрузка по моногидрату на 1 агрегат, кг \ час.
5342,08 \ 4,5 = 1187,12 кг \ час HNO3
Определяем расходный коэффициент по кислороду на 1000 кг моногидрата азотной кислоты.
G(O2)\G(HNO3) (5.2)
Где: G(O2) – количество кислорода, поступающего с аммиачно-воздушной смесью, кг \ час.
18389,44 \ 4,5 = 4086,54 кг \ час HNO3
Определяем расходный коэффициент по азоту на 1000 кг моногидрата азотной кислоты.
G(N2)\G(HNO3) (5.3)
Где: G(N2) – количество азота, поступающего с аммиачно-воздушной смесью, кг \ час.
60532,08\ 4,5 = 13451,57 кг \ час.
Заключение
В данном курсовом проекте было рассмотрено производство слабой азотной кислоты комбинированным методом с детальной разработкой котла-утилизатора.
Параметры рассчитанного котла-утилизатора:
Диаметр – 2500 мм
Высота – 5750 мм
Поверхность теплообмена – 840 м2
Длина трубок – 6000 мм
Диаметр штуцера для отвода пара – 450 мм
Диаметр штуцера для подачи питательной воды – 100 мм
Диаметр штуцера для ввода нитрозных газов – 600 мм
Список использованных источников
1) Дыбина П.В., Вишняк Ю.Л., Соловьева А.С. «Расчеты по технологии неорганических веществ» - М. Химия, 1987 г.
2) Мельников Е.Я. «Справочник азотчика» - М.: Химия, 1987 г.
3) Мельников Е.Я., Салтынова В.П., Наумова А.М., Блинова Ж.С. «Технология неорганических веществ и минеральных удобрений» - М.: Химия, 1983 г.
4) Шкатов Е.Ф., Шувалов В.В. «Основы автоматизации технологических процессов химических производств» - М.: Химия, 1988 г.
Похожие работы
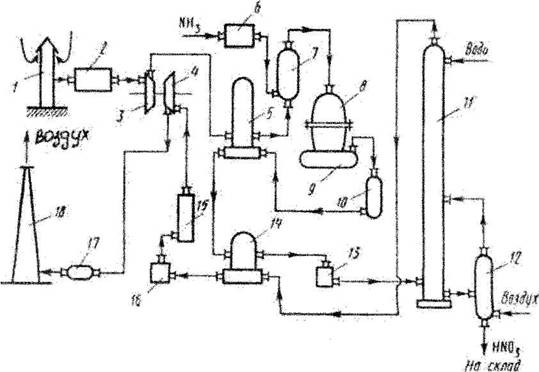
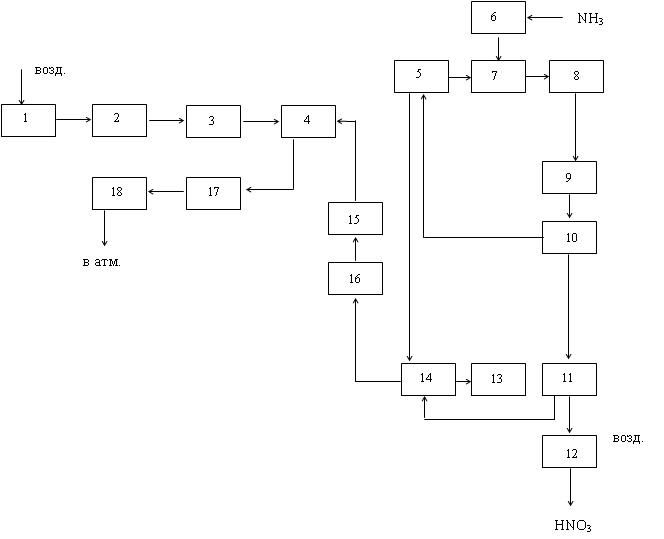
... + 50 2 = 4NO + 6Н2О 2NO+O2=2NO2 3NO2 + H2O = 2NО3 + N0 NH3 + 2О2 = HNO3 + Н2О + 421,2 Технологическая схема Рис. 3. Технологическая схема производства азотной кислоты 1-воздухозаборная труба; 2-воздухоочиститель; 3-газовый компрессор; 4-газовая турбина; 5-воздухоподогреватель; 6-испаритель аммиака; 7-смеситель с фильтром; 8-контактный аппарат; 9,17-котёл-утилизатор; 10-окислитель с ...
... в производстве концентрированной азотной кислоты по методу прямого синтеза. В отдельных случаях используется для обогащения АВС при получении неконцентрированной азотной кислоты. СОВРЕМЕННОЕ СОСТОЯНИЕ ТЕХНОЛОГИИ ПРОИЗВОДСТВА НЕКОНЦЕНТРИРОВАННОЙ АЗОТНОЙ КИСЛОТЫ. Азотная кислота и главным образом ее природная соль - натриевая селитра известны с давних времен. В 778 г. Арабский ученый Гебер ...
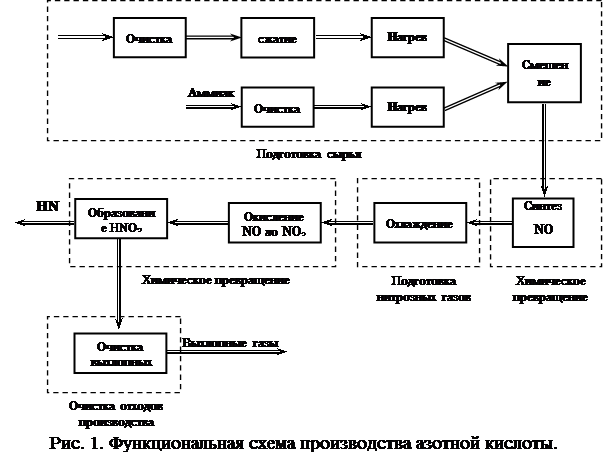
... очистки выхлопных газов, выпускающий продукцию в виде 53–58% -ной HNO3. Технологическая схема этого производства в упрощенном варианте представлена на рисунке 5. Подготовка сырья Рис.5 Схема производства азотной кислоты под давлением 0,716 МПа с приводом компрессора от газовой турбины: 1 – фильтр воздуха; 2 – реактор каталитической очистки; 3 – топочное устройство; 4 – ...
... способствует образованию NO2. При температурах до 100 ºС равновесие реакции практически полностью сдвинуто в правую сторону. Окисление диоксида азота – самая медленная стадия получения азотной кислоты. Она сильно зависит от концентрации реагентов, давления температуры. Применение воздуха, обогащенного кислородом (или чистого кислорода) позволяет получать НГ[2] с повышенным содержанием ...




0 комментариев