Навигация
Концентрации или парциальные давления окисленной и восстановленной форм
2. Концентрации или парциальные давления окисленной и восстановленной форм.
Качественно ясно по принципу Ле Шателье: чем выше концентрация окисленной формы и чем ниже концентрация восстановленной, тем сильнее эта система притягивает электроны, т.е. тем выше j. Количественную зависимость дает уравнение В. Нернста (без вывода):
j = j0 + (RT/nF) ln([Ox]/[Red]), где
R и T - газовая постоянная и абс. температура, n - число электронов, передаваемых в электродной реакции, [Ox] - концентрация (точнее, активность) или давление окисленной формы в степени, соответствующей коэффициенту в уравнении, причем здесь учитывается не только сам окислитель, но вообще все реагенты, стоящие в одной стороне уравнения с окислителем, а [Red] - то же для восстановленной формы, j0 - стандартный электродный потенциал. Как всегда, если вещество составляет отдельную твердую или жидкую фазу, его активность по определению равна единице и не пишется; если вещество растворено, то подставляется его молярная концентрация, а стандартным состоянием является 1 М раствор; если вещество плохорастворимое, то стандартное состояние - его насыщенный раствор, то есть опять-таки равновесие с отдельной фазой растворяемого вещества, а если вещество в газовой фазе, то ставится его парциальное давление в атмосферах, а стандартное состояние - 1 атм. Если все реагенты и продукты - в стандартных состояниях, то под логарифмом 1, второе слагаемое =0, и j = j0. Если подставить коэффициент перехода от натуральных к десятичным логарифмам, числовые значения R и F и принять Т = 298 К, то
j = j0 + (0,0591В/n)lg([Ox]/[Red]).
Примеры.
j(Zn2+/Zn) = j0 + (0,0591B/2)lg[Zn2+] - без знаменателя; j(H+/H2) = j0 + (0,0591B/2)lg[H+]2/p(H2).
Для реакции MnO4- +8H+ +5e = Mn2+ + 4H2O j = j0 + (0,0591B/5)lg([MnO4-][H+]8/[Mn2+]). Заметьте, что число электронов здесь подсчитано по закону сохранения заряда (без них суммарный заряд ионов слева +7, справа +2) и не требует представления о том, что в перманганате степень окисления марганца 7. Степень окисления - условное понятие, а 5е в этой реакции определяются объективно.
3. Температура. В уравнении Нернста она влияет в двух местах: ведь и стандартный потенциал сам может зависеть от температуры, поэтому однозначно предсказать вид зависимости сложно, но она, безусловно, есть. В справочниках чаще всего приводят стандартные потенциалы при 298 К.
4. Зависит ли j от способа записи уравнения электродной реакции? Мы знаем, что, если умножить левую и правую части химического уравнения на один и тот же коэффициент b, то соответствующие DН, DS, DG увеличиваются в b раз, а К равновесия возводится в степень b. В уравнении Нернста при этом выражение под логарифмом будет возведено в степень b, а число электронов тоже возрастет в b раз. Если вынести показатель из-под знака логарифма, он сократится - и потенциал останется тем же.
Докажем то же иначе. Убыль энергии Гиббса -DG - это работа химической реакции: -DG = А = nFe. Мы увеличиваем DG и n в одинаковое число раз, e не меняется.Если поменять местами левую и правую части уравнения, то DН, DS, DG меняют знак, а К равновесия превращается в обратную величину. С потенциалом же ничего не происходит. Он характеризует не прямую и не обратную реакцию, а состояние их равновесия. Показания вольтметра не изменятся, если переписать уравнение наоборот. Плюс останется плюсом. Поэтому менять знак потенциала (как в учебнике Я.А. Угая) - это грубая ошибка.
Электродные потенциалы не зависят от формы записи уравнения. Но стандартные электродные потенциалы могут зависеть от формы записи, так как там могут подразумеваться разные стандартные состояния. Если в уравнении стоит Cl2(р-р), значит стандартным состоянием является 1 М раствор, а если Cl2 - то парциальное давление хлора 1 атм. Это разные состояния - разные f. Одно и то же окислительно-восстановительное уравнение можно записать для разных сред, например:
MnO4- +4H+ +3e = MnO2Ї+ 2H2O; j° = 1,69 В;
MnO4- + 2H2O +3e = MnO2Ї + 4 ОН-; j° = 0,60 В.
Почему разные потенциалы? В первом случае под стандартным состоянием понимается состояние с [H+] = 1 моль/л (рН = 0), а во втором - с [ОH-] = 1 моль/л (рОН = 0, а рН = 14). Для любого конкретного рН одно и то же значение j получается из обоих уравнений. Это не разные процессы, а один и тот же, записанный по разным стандартам.
До сих пор речь шла о равновесных потенциалах.
Но если через электрод идет ток, то потенциал отклоняется от равновесного. Это явление называется поляризация электрода. Наиболее очевидная (но не единственная) причина поляризации - изменение концентрации реагентов вблизи электрода. У анода возрастает концентрация окисленной формы и уменьшается концентрация восстановленной, и диффузия не успевает их выравнивать по объему раствора, поэтому, согласно уравнению Нернста, потенциал анода увеличивается по сравнению с тем, который соответствует средним по объему концентрациям. И чем больше плотность тока (сила тока на единицу площади), тем сильнее отклонение потенциала от равновесного. На катоде, где идет восстановление, наоборот, растет концентрация восстановленной формы и падает концентрация окисленной, потенциал катода уменьшается. В гальваническом элементе jк>jА, поэтому напряжение U получается меньше эдс. И чем больший ток мы хотим получить от батарейки, тем меньше ее напряжение. Наоборот, при электролизе jк<jА, поэтому, чтобы процесс шел с большой скоростью, приходится прикладывать напряжение больше равновесного. Посмотрим еще раз на медно-цинковый гальванический элемент. Поскольку концентрации растворов близки к стандартным, его эдс должна соответствовать разности стандартных потенциалов медного и цинкового электродов: 0,34В - (-0,76В) = 1,10 В. Реально получается небольшое отклонение - из-за того, что сопротивление вольтметра не бесконечно, и ток через него все же идет, и из-за неточности концентраций. Да и температура не точно 298 К.
Обязательно ли в гальваническом элементе погружать металл в раствор его соли? Вовсе нет, в источниках тока часто используют другие электролиты. Но если мы погружаем цинк в раствор, где концентрация его ионов равна нулю, то получаем из уравнения Нернста потенциал -Ґ. Смысла в этом нет. Электрод с таким потенциалом мгновенно начинает окисляться, в растворе появляются ионы цинка, их концентрация быстро растет, и потенциал нестабилен. Поэтому для наглядности мы используем заданную и довольно большую концентрацию, которая уже не может сильно измениться.
НАПРАВЛЕНИЕ ОВР
Окислительно-восстановительную реакцию можно (хотя бы мысленно) разложить на две полуреакции - окисление восстановителя и восстановление окислителя. Каждой полуреакции с участием электролита соответствует свое значение электродного потенциала (еще его называют редокс-потенциал). Электроны заряжены отрицательно, поэтому они будут стремиться перейти от системы с меньшим j к системе с большим j. ОВР идет самопроизвольно, если у предполагаемого окислителя j больше, чем у предполагаемого восстановителя. Если же мы пытаемся использовать в роли окислителя систему с меньшим j, то реакция не пойдет. Другой вариант рассуждений. Эдс ОВР равна j окислителя - j восстановителя. А DG = -nFe. Чтобы реакция шла самопроизвольно, нужно DG<0, то есть эдс e >0.
Для ОВР, как для любой реакции, DG° = -RTlnK. Тогда -RTlnK = -nFe°, lnK = nFe°/RT, K = exp(nFe°/RT), где e° = j°ок-ля - j°восст-ля - стандартная эдс реакции.
Пример. Возможна ли какая-нибудь ОВР между металлической медью и водным раствором соли железа (3+)? Выпишем возможные полуреакции и найдем в справочнике соответствующие j°. Обратите внимание, что все уравнения полуреакций записываются в стандартной форме как восстановление окислителя со знаком обратимости. Реально, конечно же, в той системе, где j меньше, будет идти обратный процесс - окисление.
(1) Fe3+ + e = Fe2+; j°1 = 0,77 В;
(2) Fe3+ + 3e = Fe; j°2 = - 0,04 В;
(3) Cu 2+ +e = Cu; j°3 = 0,34 В;
j°2 << j°3 <<j°1. Это значит, что вторая система не может быть окислителем, реакция 2Fe3+ + 3Cu = 2Fe + 3Cu2+ не идет. Точнее, ее константа равновесия ничтожно мала: К = exp(-0,38*6/0,059) » 10-17 при 298К. Но первая система может окислять медь, и реакция 2Fe3+ + Cu = 2Fe2+ + Cu2+ идет. Ее константа равновесия К = exp(+0,43*2/0,059) »106 при 298К. Полуреакция (1) идет в прямом направлении, а полуреакция (3) с меньшим j°- в обратном.
Влияние рН на окислительно-восстановительные свойства и направление ОВР
В водных растворах концентрация ионов водорода меняется в очень широких пределах - от нескольких моль/л в кислых растворах до 10-14 - 10-15 моль/л в щелочных, то есть на 15 порядков. Поэтому, если в ОВР образуются или расходуются ионы водорода или гидроксила, то рН очень сильно влияет на направление таких реакций. Рассмотрим на примере трех вариантов восстановления перманганата.
(1) MnO4- +8H+ +5e = Mn2+ + 4H2O; j01 = 1,51 В;
(2) MnO4- +4H+ +3e = MnO2 + 2H2O; j02 = 1,69 В;
(3) MnO4- + e = MnO42-; j03 = 0,56 В.
j1 = j°1 + (0,0591B/5)lg([MnO4-][H+]8/[Mn2+]) = 1,51В + (0,0591B/5)lg([MnO4-]/[Mn2+]) - (8*0,0591/5)pH. Если принять стандартными все концентрации, кроме рН, то
j1 = 1,51В -0,0946В*рН. При рН=7 это дает 0,85В.
Аналогично j2 = 1,69В - 0,0788рН, при рН=7 получается 1,14В, а при рН=14 = 0,59В.
Постройте на одном графике зависимости потенциалов трех систем от рН. Уравнения линейные, поэтому достаточно вычислить j при двух значениях рН (например, 0 и 14) и соединить прямой (прямую 1 довести только до pH=6, т.к. дальше осаждается Mn(OH)2).
Только у третьей системы потенциал не зависит от рН, а у двух других резко падает с ростом рН, то есть окислительные свойства перманганата сильнее всего выражены в кислой среде, а в щелочной его труднее восстановить и, наоборот, соединения низших степеней окисления легче окислить.
Система 3 является самым слабым окислителем и по потенциалу, и по числу принимаемых электронов. Поэтому третий вариант восстановления реализуется только в очень сильно щелочной среде, где получается j3 > j2, и только при недостатке восстановителя. Если же восстановителя достаточно, то будет идти процесс 2. Процесс 2 по потенциалу предпочтительнее, чем 1, но уступает по числу электронов. Более строгим критерием направления процесса будет DG.
Рассмотрим, например, эти три варианта при окислении иодида до иода: I2Ї +2e = 2I-. Стандартный потенциал этого восстановителя, независимо от рН, 0,54В. (А у другого восстановителя потенциал может тоже зависеть от рН).
(1) 2MnO4- + 16H+ +10 I- = 4Mn2+ + 8H2O + 5 I2Ї; n=10;
(2) 2MnO4- + 8H+ + 6I- = 2MnO2 + 4H2O + 3I2Ї; n=6;
(3) 2MnO4- + 2I- = 2MnO42- + I2Ї; n=2;
Выразим эдс этих трех систем через рН, принимая все прочие концентрации стандартными.
e1 = 1,51 - 0,54 + 0,00591lg[H+]16 = 0,97 - 0,0946pH (B); DG = -nFe; D1G/F = -9,7 + 0,946pH (B);
e2 = 1,69 - 0,54 + (0,0591/6)lg[H+]8 = 1,15 - 0,0788pH (B); D2G/F = -6,9 + 0,473pH (B)
e3 = 0,56 - 0,54 = 0,02(B) независимо от рН; D3G/F = - 0,04 B.
Наиболее выгодна та из реакций, у которой меньше DG в расчете на одно и тоже количество вещества (здесь - на 2 моль перманганата). Если в уравнениях конкурирующих реакций разные коэффициенты, то сначала надо их домножить так, чтобы они стали одинаковыми, а потом уже сравнивать DG. Реакции 1 и 2 равновероятны, если D1G=D2G. Решив это уравнение относительно рН, получаем рН=5,9. При меньших рН D1G<D2G, при больших - наоборот. Аналогично, приравняв D3G=D2G, найдем рН=14,5.
Вывод: если восстановитель в избытке, то в стандартных условиях вариант 1 термодинамически выгоднее в кислой среде (рН<5,9), вариант 2 - в нейтральной и щелочной (5,9<рН<14,5), а вариант 3 - лишь в очень сильно щелочной среде (рН>14,5).
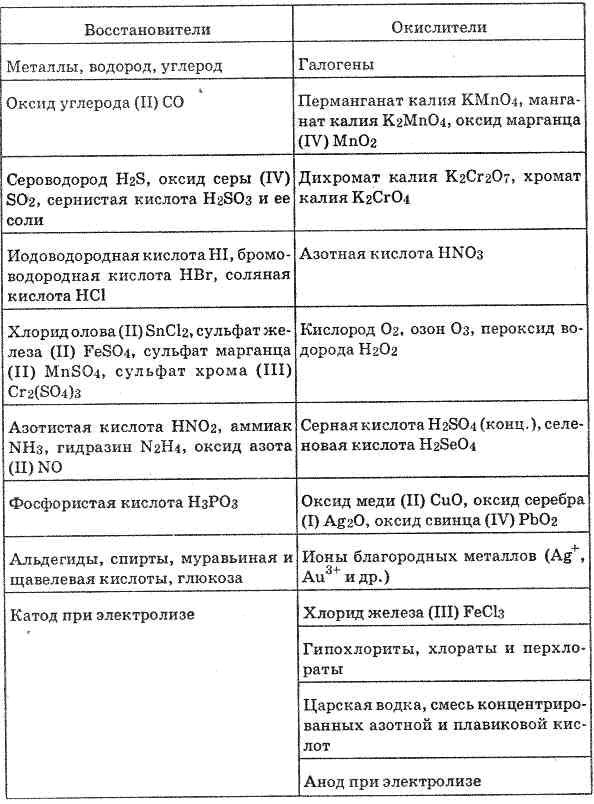
Окислительно-восстановительные реакции (ОВР) (реакции окисления-восстановления) происходят с изменением степени окисления атомов, входящих в состав реагирующих веществ. При окислении веществ степень окисления элементов возрастает, при восстановлении - понижается.
Первоначально окислением называли только реакции веществ с кислородом, восстановлением - отнятие кислорода. С введением в химию электронных представлений понятие окислительно-восстановительных реакций было распространено на реакции, в которых кислород не участвует.
В неорганической химии окислительно-восстановительные реакции (ОВР) формально могут рассматриваться как перемещение электронов от атома одного реагента (восстановителя) к атому другого (окислителя), например:
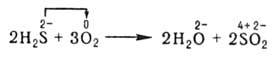
При этом окислитель восстанавливается, а восстановитель - окисляется. При протекании реакций в гальваническом элементе переход электронов осуществляется по проводнику, соединяющему электроды элемента, и изменение энергии Гиббса ДG в данной реакции может быть превращено в полезную работу. В отличие от реакций ионного обмена окислительно-восстановительные реакции (ОВР) в водных растворах протекают, как правило, не мгновенно.
При окислительно-восстановительных реакциях атомы в высшей степени окисления являются только окислителями, в низшей - только восстановителями; атомы в промежуточной степени окисления в зависимости от типа реакции и условий ее протекания могут быть окислителями или восстановителями. Многие окислительно-восстановительные реакции (ОВР) - каталитические По формальным признакам окислительно-восстановительные реакции (ОВР) разделяют на межмолекулярные (например, 2SO2 + O2 → SO3) и внутримолекулярные, например:
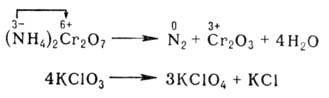
Последняя реакция представляет собой самоокисление-самовосстановление (см. Диспропорционирование).
окислительно-восстановительные реакции (ОВР) часто сопровождаются высоким энерговыделением, поэтому их используют для получения теплоты или электрической энергии. Наиболее энергичные окислительно-восстановительные реакции (ОВР) протекают при взаимодействии восстановителей с окислителями в отсутствие растворителя; в растворах такие реакции могут быть невозможны вследствие окислительно-восстановительного взаимодействия одного или обоих реагентов с растворителем. Так, в водном растворе нельзя непосредственно провести реакцию 2Na + F2 → 2NaF, поскольку натрий и фтор бурно взаимодействуют с водой. На окислительно-восстановительные свойства ионов сильно влияет комплексообразование, например: комплекс [Co2+(CN)6]4-, в отличие от гидратированного иона Со2+, является сильным восстановителем.
В случае окислительно-восстановительных реакций в органической химии использование обобщенной концепции окисления-восстановления и понятия о степени окисления часто малопродуктивно, особенно при незначительно полярности связей между атомами, участвующими в реакции. В органической химии окисление рассматривают обычно как процесс, при котором в результате перехода электронов от органического соединения к окислителю возрастает число (или кратность) кислородсодержащих связей (С — О, N — О, S — О и т.п.) либо уменьшается число водородсодержащих связей (С — Н, N —Н, S —Н и т.п.), например: RCHO → RCOOH; R2CHCHR2 → R2C=CR2. При восстановлении органических соединений в результате приобретения электронов происходят обратные процессы, например: R2CO → R2CH2; RSO2Cl → RSO2H.
Используют также подход, при котором атомам С в молекуле приписывают различные степени окисления в зависимости от числа связей, образованных с элементом более электроотрицательным, чем водород. В этом случае функциональные производные можно расположить в порядке возрастания их степени окисления. Так, насыщенные углеводороды относят к нулевой группе (приблизительная степень окисления — 4), R2C=CR2, ROH, RCl и RNH2 - к первой (- 2), RCCR, R2CO и R2CCl2 - ко второй (0), RCOOH, RCCCl, RCONH2 иRССl3 - к третьей (+2), RCN, CCl4 и СО2 - к четвертой (+4). Тогда окисление - процесс, при котором соединение переходит в более высокую категорию, а восстановление - обратный процесс.
Механизмы окислительно-восстановительных реакций весьма разнообразны; реакции могут протекать как по гетеролитическому, так и по гомолитическому механизму. Во многих случаях начальная стадия реакции - процесс одноэлектронного переноса. Окисление обычно протекает по положениям с наибольшей электронной плотностью, восстановление - по положениям, где электронная плотность минимальна. В органической химии используют широкий ряд восстановителей и окислителей, что позволяет выбрать реагент, обладающий селективностью (т.е. способностью действовать избирательно на определенные функциональные группы), а также получать продукты в требуемой степени окисления. Например, борогид Na восстанавливает кетоны или альдегиды до спиртов, не реагируя с амидами и сложными эфирами; LiAlH4 восстанавливает все эти соединения до спиртов. Среди окислителей высокой селективностью обладают, например, комплекс CrО3 с пиридином, с высоким выходом окисляющий спирты в кетоны, не затрагивая кратные связи С—С, а также SeO2, окисляющий кетоны и альдегиды до б-дикарбонильных соединений.
Селективность окислительно-восстановительных реакций может быть обеспечена и в каталитических процессах; например, в зависимости от катализатора и условий реакций ацетиленовые углеводороды можно селективно гидрировать до этиленовых или насыщенных углеводородов (см. Гидрирование). Электрохимическое восстановление СО2 до СО в водной среде в присутствии никелевого комплекса 1,4,8,11-тетраазациклотетрадекана позволяет проводить желаемый процесс при более низких потенциалах и одновременно подавлять электролиз воды с образованием Н2. Эта реакция имеет ключевое значение для превращения СО2 через СО в разнообразные органические вещества.
Каталитические окислительно-восстановительные реакции (ОВР) играют важную роль в промышленности, например:
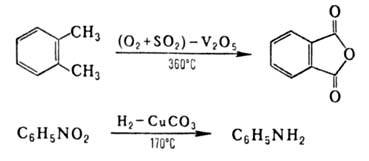
окислительно-восстановительные реакции (ОВР) широко распространены в природе и используются в технике. В основе жизни лежат окислительно-восстановительные реакции (ОВР), происходящие при фотосинтезе, дыхании, транспорте электронов; они же обеспечивают основную часть энергопотребления человечества за счет сжигания органического топлива. Получение металлов, извлечение энергии взрыва основано на окислительно-восстановительных реакциях.
Классификация окислительно-восстановительных реакций
Реакции межмолекулярного окисления-восстановления – это реакции, в которых атом-окислитель и атом-восстановитель принадлежат разным веществам. Эти вещества могут быть как простыми, так и сложными.
4N3-H3 + 3O02 ® 2N02 + 6H2O2-
![]() 2N3-
- 6e ®
N02 2 восстановитель
2N3-
- 6e ®
N02 2 восстановитель
O02 + 4e ® 2O2- 3 окислитель
Реакции внутримолекулярного окисления-восстановления – это реакции, в которых атом-окислитель и атом-восстановитель входят в состав одной и той же молекулы или одного и того же иона.
Например, разложение хлората калия
![]() 2KCl5+O2-3
® 2KCl-
+ 3O02
2KCl5+O2-3
® 2KCl-
+ 3O02
Cl5+ + 6e ® Cl- 2 окислитель
2O2- -4e ® O02 3 восстановитель
Реакции диспропорционирования (самоокисление– самовосстановление) - это реакции, в которых функцию окислителя и восстановителя выполняет один и тот же атом молекулы или иона, находящийся в промежуточной степени окисления. Например:
![]()
![]() 4KCl5+O3
® 3
KCl7+O4
+ KCl-
4KCl5+O3
® 3
KCl7+O4
+ KCl-
Cl5+ - 2e ® Cl7+ 6 3 восстановитель
Cl5+ +6e ® Cl- 2 1 окислитель
Реакции конмутации – реакции внутримолекулярного окисления- восстановления, в результате которых происходит выравнивание степеней окисления атомов одного и того же элемента. Например:
N3-H4N5+O3 = N21+O + 2H2O
Влияние среды на протекание окислительно-восстановительных реакций
Реакции окисления-восстановления могут протекать в различных средах (кислой, нейтральной и щелочной), при этом в зависимости от среды может изменяться характер протекания реакции между одними и теми же веществами. Рассмотрим взаимодействие перманганата калия с сульфитом калия в различных средах.
а) Кислая среда:
2KMn7+O4 + 5K2S4+O3 + 3H2SO4 ® 2Mn2+SO4 + 6K2S6+O4 + 3H2O
![]() Mn7+
+ 5e ® Mn2+ 2
Mn7+
+ 5e ® Mn2+ 2
S4+ - 2e ® S6+ 5
б) Нейтральная среда:
2KMn7+O4 + 3K2S4+O3 + H2O ® 2Mn4+O2 + 3K2S6+O4 + 2KOH
![]() Mn7+
+ 3e ® Mn4+ 2
Mn7+
+ 3e ® Mn4+ 2
S4+ - 2e ® S6+ 3
в) Щелочная среда:
2KMn7+O4 + K2S4+O3 + 2KOH ® K2Mn6+O4 + 2K2S6+O4 +H2O
![]() Mn7+
+ e ® Mn6+ 2
Mn7+
+ e ® Mn6+ 2
S4+ - 2e ® S6+ 1
Схематически это можно представить следующим образом:
Окисленная Восстановленная форма
Форма
![]()
![]() Mn2+
- бесцветный
Mn2+
- бесцветный
![]() Mn7+
® MnО2 -
бурый осадок
Mn7+
® MnО2 -
бурый осадок
![]() MnО42-
- зеленый
MnО42-
- зеленый
Особые случаи составления уравнений окислительно-восстановительных реакций
Рассмотренная методика составления окислительно-восстановительных реакций применима к большинству простых и сложных процессов. Но в некоторых специальных случаях необходимы дополнительные пояснения.
1. Если число электронов, отдаваемое восстановителем, и число электронов, присоединяемое окислителем, имеют общий наибольший делитель, то при нахождении коэффициентов оба числа делят на него. Например, в реакции
HCl7+O4 + 4S4+O2 + 4H2O = 4H2S6+O4 + HCl1-
основными коэффициентами для восстановителя и окислителя будут не 6 и 2, а 4 и 1.
Если число участвующих в реакции электронов нечетно, а в результате получается четное число атомов, то коэффициенты удваиваются. Например, в реакции
2Fe3+Cl3 + 2HJ1- = J20 + 2Fe2+Cl2 + 2HCl
основными коэффициентами будут не 1 и 1, а 2 и 2.
Похожие работы
... подкрепляет своим одобрением неправильный или не вполне точный ответ ученика. 1.2 Совершенствование школьного химического эксперимента при проблемном обучении 1.2.1 Принципы разработки методической системы и содержания опытов по химии в системе проблемного обучения Характерной особенностью развивающего обучения является широкое использование проблемного подхода, который включает создание ...
ависимо от способа получения и места нахождения. 2. Строение внешнего электронного уровня атома калия и кальция. 1 правило Клечковского. Строение внешнего электронного уровня атома скандия. 2правило Клечковского У атома аргона остаются незанятыми все орбитали 3d-подуровня. Однако у следующих за аргоном элементов – калия и кальция – заполнение 3-го электронного слоя временно прекращается, и ...
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...
... учреждение страны, а в ее задачи входило усовершенствование наук, просвещение, а также усовершенствование мануфактур, ремесел и фабрик. В то же время в начале XIX столетия, особенно после Отечественной войны 1812 г., в развитии химии в России появились новые черты. Смена мануфактурного производства фабрично-заводским выдвинула перед учеными множество практических задач, связанных с рациональной ...
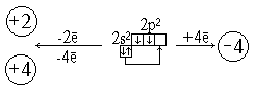
0 комментариев