Навигация
Растворимость веществ. Произведение растворимости. Механизм накипеообразования
28. Растворимость веществ. Произведение растворимости. Механизм накипеообразования
Растворимость вещества — способность образовывать с другим веществом однородную, термодинамически устойчивую систему переменного состава, состоящую из двух или большего числа компонентов. Такие системы возникают при взаимодействии газов с жидкостями, жидкостей с жидкостями и т.д. (см. Растворы).Соотношение компонентов может быть либо произвольным, либо ограниченным некоторыми пределами. В последнем случае Р. называют ограниченной. Мерой Р. вещества при данных условиях служит концентрация его насыщенного раствора. Р. различных веществ в определённом растворителе зависит от внешних условий, прежде всего — от температуры и давления. Давление наиболее сильно сказывается на Р. газов. Изменение внешних условий влияет на Р. в соответствии с принципом смещения равновесий (см. Ле Шателье — Брауна принцип).Для наиболее важных растворителей составлены таблицы Р. различных веществ в зависимости от внешних условий или только для стандартных условий.
Произведение растворимости — произведение концентраций ионов в насыщенном растворе малорастворимого сильного электролита. Показатели степени для концентраций, входящих в П. р., равны коэффициенту при соответствующем ионе в уравнении диссоциации электролита. Для неидеальных растворов концентрации должны быть заменены на активности и полученное произведение называется произведением активностей. При данной температуре и в данном растворителе П. р. для каждого электролита есть характерная постоянная величина.
Постоянство П. р. выводится из действующих масс закона и представляет собой частную форму этого закона в приложении к равновесию твёрдый электролит Ы его насыщенный раствор. При этом предполагается, что в растворе электролит находится в полностью диссоциированной форме. П. р. наиболее точно измеряется методом эдс. Часто для измерения П. р. используют также определение растворимости по электропроводности насыщенных растворов. Для многих соединений П. р. установлено с достаточной для практических целей точностью. В таблицах П. р. обычно приводятся при температуре 25 °С (иногда при 18 °С).Из правила постоянства П. р. следует, что если произведение концентраций ионов в растворе превышает величину П. р., то выпадает осадок; в противном случае осадок не образуется. Это следствие позволяет регулировать содержание ионов в растворе при использовании процессов осаждения, растворения, а также высаливания, имеющих большое значение в аналитической химии и химической технологии. Так, при увеличении концентрации одного из ионов путём введения в раствор нового электролита с одноимённым катионом или анионом концентрация др. иона понижается за счёт выпадения части труднорастворимого электролита в осадок. Понижение растворимости происходит обычно лишь до некоторого минимального значения, после чего может наблюдаться вновь повышение растворимости из-за образования комплексных ионов или увеличения ионной силы раствора. Повышения растворимости можно достигнуть, связывая один из ионов в растворе, так что образуется др. ион, который не даёт малорастворимого соединения. Например, для перевода в раствор осадка СаСО3 ион связывают с помощью иона Н+ в слабо диссоциированный ион : ; концентрация ионов при этом уменьшается и осадок растворяется до тех пор, пока не будет достигнуто П. р.
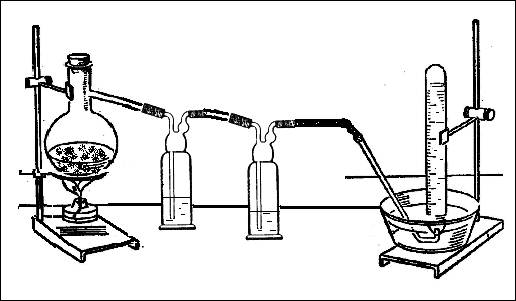
Сероводородный метод анализа, метод химического качественного анализа смеси ионов металлов (главным образом катионов) в водных растворах. Метод основан на неодинаковой растворимости хлоридов, гидроокисей, карбонатов и сульфидов металлов.
С. м. а. предполагает классификацию ионов металлов, представленную в таблице. Существуют и другие классификации ионов металлов. Применяя т. н. групповые реагенты — осадители (HCl, H2S, (NH4)2S, (NH4)2CO3), последовательно разделяют сложную по составу смесь ионов металлов на пять аналитических групп.Ход систематического анализа следующий: добавлением HCl выделяют ионы V группы. Из фильтрата (pH около 3) осаждают катионы IV группы пропусканием H2S. Затем действием избытка (NH4)2S переводят в осадок катионы III группы. Оставшуюся в растворе смесь катионов II и I групп разделяют прибавлением раствора (NH4)2CO3. После этого каждую группу катионов разделяют на подгруппы и обнаруживают ионы химическими реакциями.С. м. а. применяется для предварительной идентификации неизвестного по составу вещества с целью выбора наиболее рационального пути его количественного анализа. Количественный С. м. а. иногда используется при анализе сложных по составу материалов.
Накипеобразование на поверхностях нагрева. В процессе работы котла в котловой воде протекают различные физико-химические процессы, обусловливающие разрушение одних соединений и образование других. Это приводит к возникновению веществ с различной степенью растворимости. Труднорастворимые вещества выделяются из воды в виде осадка, образующего при определенных условиях накипь или шлам.
Накипью называют плотные отложения, возникающие на поверхности нагрева. К шламу относятся выпадающие вещества в виде подвижного осадка, которые могут также образовывать вторичную накипь, прикипая к поверхности труб.
Образование осадка в виде накипи или шлама происходит при наличии пересыщенного раствора, т. е. высокой концентрации солей. Испарение котловой воды, подача питательной и добавочной воды с более высокой минерализацией создают благоприятные условия для этого процесса. Произведение концентраций находящихся в растворе ионов труднорастворимого вещества называется произведением растворимости, т.е.
ПР = СКТСАН где СКТ,САН— концентрация соответственно катиона и аниона труднорастворимого соединения. Произведение концентраций при данной температуре является постоянной величиной и, если СКТСАН > ПР, происходит выпадение осадка (твердой фазы). Образующиеся в толще воды кристаллические частицы осаждаются на поверхности нагрева в виде слоя накипи или остаются во взвешенном состоянии как подвижный шлам. Накипь может появиться в результате увеличения концентрации одного из ионов, образующих труднорастворимые соединения, что является следствием химических процессов.Таким образом, низкое содержание Са в воде еще не означает, что не будет кальциевых отложений.Наибольшее влияние на процесс накипеобразования оказывают катионы Са2+ и Mg2+ и анионы С2-3, ОН-, SO2-4, SiO2-3. Определенные сочетания этих катионов и анионов в виде солей представляют собой труднорастворимые вещества. Накипеобразующими соединениями, например, являются: карбонат кальция и магния (СаСО3, MgCO3), гидрат магния (Mg(OH)2), сульфат кальция (CaSO4), силикаты кальция и магния СаSiO3, MgSiO3).
Карбонат кальция образуется в результате нагрева из бикарбоната:
Са(НСО3)2→СаСО3 +H2O+СО2.
Повышение концентрации в воде углекислоты СО2 может смещать равновесие реакции влево, т. е. ведет к образованию бикарбоната. Однако для котловой воды, где идет процесс кипения и СО2 удаляется, наиболее характерен переход Са(НСО3)2 в карбонат СаСО3.
Аналогичная реакция идет и с бикарбонатом магния при нагревании: Mg(HCO3)2 → MgCO3 + Н2О + СО2.
При нагревании воды с высокой щелочностью происходит гидролиз карбоната магния с образованием труднорастворимого соединения гидроокиси магния: MgCO3 + 2Н2О → Mg(OH)2 + H2CO3.
Карбонаты кальция образуют в котле карбонатную накипь. С повышением щелочности воды они осаждаются в грубодисперсном состоянии и входят в состав шлама.
Соединение Mg(OH)2 находится в воде преимущественно в виде шлама и может образовывать вторичную накипь (прикипание осаждающегося шлама).
Силикаты CaSiO3 и MgSiO3 в природной воде находятся в коллоидальной форме в небольшом количестве. Однако в случае образования силикатной накипи на поверхности нагрева слой загрязнения становится прочным, трудноудаляемым.
Одной из причин образования насыщенных растворов и выпадения осадка является понижение растворимости некоторых соединений при повышении температуры воды. Такие соединения имеют отрицательный коэффициент растворимости. К ним относятся СаСО3, CaSO4, Mg(OH)2, CaSiO4, MgSiO3.
Вторичную накипь могут образовывать продукты коррозии металла, заносимые в котел с питательной водой.
29 Окислительно-восстановительные реакции (ОВР), их классификация. Важнейшие окислители и восстановители. Составление уравнений ОВР по методу полуреакций. Влияние среды на протекание ОВР
ОКИСЛИТЕЛЬНО-ВОССТАНОВИТЕЛЬНЫЕ РЕАКЦИИ (ОВР)
ОВР – реакции, в которых изменяются степени окисления элементов, то есть электроны переходят от одного атома или вещества (восстановителя) к другому (окислителю).
А степень окисления – это заряд, который имел бы атом, если бы все образованные им полярные связи стали ионными. Если связи действительно ионные, то с.о. совпадает с зарядом элементарного иона, например, K+F-. Если не все связи ионные, то степень окисления – это условное понятие, не имеющее строгого смысла, но полезное.
Например, реакция С + О2 = СО2 считается ОВР, т.к. в простых веществах степени окисления нулевые, а в СО2 углероду приписывается с.о. +4, а кислороду –2, хотя ионов С+4 и О-2 там нет. Считается, что при сгорании угля электроны переходят от атомов С к атомам О, но это трудно доказать экспериментально. Это пока условность.
Но во многих случаях удается провести ОВР так, что восстановитель и окислитель разделены в пространстве, и заряды передаются через проводники. Тогда можно экспериментально зарегистрировать перенос заряда (токи, напряжения) и определить, сколько именно электронов передается. ОВР становится реальным, а не условным, понятием. Такие процессы изучает ЭЛЕКТРОХИМИЯ. Подробно – в курсе ФХ, а сейчас очень кратко. Ключевое понятие электрохимии –
ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
Электрод – это электронный проводник (металл или полупроводник, твердый или жидкий), находящийся в контакте с электролитом, т.е. ионным проводником (раствором, расплавом или твердым). При этом на границе раздела фаз возникает скачок электрического потенциала – электродный потенциал. Почему?
1) Ионы металла могут в некотором количестве перейти в раствор, оставив электроны в металлической фазе. СХЕМА. Этому способствуют полярные молекулы растворителя, например, воды: М(тв.) + mH2O(ж.) = [M(OH2)m]n+(ж.) + ne-(тв.). В данном примере электрод заряжается отрицательно и притягивает к себе катионы, так что они могут возвращаться обратно, и наступает равновесие. Это самопроизвольный процесс хотя бы потому, что ведет к росту энтропии.
2) Ионы из электролита, как одноименные с материалом электрода, так и посторонние, могут прилипать (адсорбироваться) на поверхности металла, сообщая ему заряд и потенциал, как положительный, так и отрицательный.Абсолютное значение потенциала j невозможно измерить: если к электроизмерительному прибору (вольтметру, потенциометру) присоединить один электрод - прибор ничего не покажет, т.к. цепь не замкнута, а чтобы замкнуть ее, нужно ввести в электролит второй электрод (СХЕМА), и там возникнет свой электродный потенциал, так что прибор покажет РАЗНОСТЬ потенциалов.
Поэтому договорились: выбрать какой-то электрод за начало отсчета, принять для него j=0, а все остальные отсчитывать от него. Точно так же в механике для расчета потенциальной энергии в поле тяготения (mgh) нужно договориться, от какого уровня отсчитывать высоту h - от уровня стола, пола, земли или моря.
В качестве такого электрода принят нормальный водородный электрод. Это пластинка из платины (покрытая мелкораздробленной “платиновой чернью” для увеличения поверхности), находящаяся в растворе с активностью ионов водорода 1 моль/л (т.е. в 1 н растворе сильной кислоты) и обдуваемая водородом под давлением 1 атм. Там, на трехфазной границе тв.-ж.-газ, устанавливается равновесие 2Н+ (ж) + 2е (тв) = Н2 (г). Платина здесь - инертный электрод, служащий для подвода и отвода электронов, но не входящий в уравнение.Система из двух электродов с разными потенциалами, соединенных электролитом, называется ГАЛЬВАНИЧЕСКИМ ЭЛЕМЕНТОМ. Гальванические элементы применяются как химические источники тока, а также для измерения потенциалов - в аналитических целях и в научных исследованиях (подробнее - в конце темы).
Демонстрация: элемент (+)CuЅр-р Cu SO4ЅЅр-р KCl ЅЅр-р ZnSO4ЅZn (-) (вертикальная черта означает границу раздела электрод-электролит, двойная черта - размытую границу разных электролитов).
Пока не вставлен солевой мостик KCl - цепь не замкнута, стрелка вольтметра стоит на нуле. Я его вставляю - стрелка отклоняется. Видно, что цинковый электрод отрицательный, т.е. служит источником электронов, которые идут по внешней цепи к медному электроду, где восстанавливаются ионы меди. Цинк окисляется, и его ионы переходят в раствор: Zn = Zn2+ +2e, ионы меди восстанавливаются, и медь осаждается на пластинке: Cu2+ +2e = Cu. В результате раствор вблизи цинка приобретает положительный заряд, а вблизи меди - отрицательный, поэтому в электролите катионы идут к меди, анионы - к цинку. Реакцию можно провести и при прямом контакте окислителя с восстановителем, но тогда вместо электроэнергии получим тепло.
Электродное равновесие - это состояние, когда на одном и том же электроде с одинаковыми ненулевыми скоростями идут восстановление и окисление, так что суммарный ток через электрод равен нулю. Если ток не равен нулю, равновесие нарушается, и потенциал отклоняется от равновесного значения. Электродвижущая сила (эдс e) гальванического элемента измеряется в равновесных условиях и равна разности равновесных потенциалов: e = j1 - j2. Но для этого нужно, чтобы сопротивление вольтметра было бесконечно велико. Если оно невелико, то в цепи течет заметный ток, равновесие нарушается, и измеряемое напряжение U < e. Эдс - это работа А по перемещению единичного электрического заряда по всей цепи: А = e*q. Если реагирует моль вещества, и каждая молекула или ион отдает или принимает ne, то q = NAne = nF, где F = eNa = 96500 Кл - число Фарадея - заряд моля электронов. А = enF.
Электрод, на котором идет окисление, называется анодом, а где идет восстановление - катодом. В гальваническом элементе анод - источник электронов, то есть имеет отрицательный знак, катод - положительный, а при электролизе все наоборот.
ФАКТОРЫ, ВЛИЯЮЩИЕ НА ЭЛЕКТРОДНЫЙ ПОТЕНЦИАЛ
1. Важнейший, конечно, это природа электрода и электролита (включая природу растворителя). Мы далее будем подробно разбирать окислительно-восстановительные свойства разных веществ, а пока - лишь некоторые соображения на простейшем примере равновесия металла с раствором его соли:
М(тв.) + m H2O(ж.) = [M(OH2)m]n+(ж.) + ne-(тв.).
На первый взгляд может показаться, что этот процесс аналогичен процессу ионизации атома: М(г.) = Мn+(г.) + ne-(г.). Энергия, необходимая для отрыва электрона от атома, называется потенциалом ионизации I (а тут - сумма n потенциалов ионизации). Чем ниже I и чем ниже j, тем легче металл отдает электроны, тем более сильным восстановителем он является. Но все же потенциал ионизации и электродный потенциал - это разные величины, они соответствуют разным процессам. В первом случае ион образуется из обособленного (газообразного) атома, а во втором - атомы связаны в твердое тело, и зачастую весьма прочно. Если бы железо или вольфрам состояли из несвязанных атомов, они бы не были такими твердыми и тугоплавкими! Для получения свободных атомов из твердого металла нужно затратить энергию атомизации. Чем она больше, тем менее активен металл. Ион тоже в первом случае - газообразный, во втором - сольватированный. При сольватации выделяется большая энергия, поэтому с увеличениемЅDсольв.НЅ восстановительные свойства усиливаются. Наконец, и электроны в первом случае газообразные, а во втором - связаны в металле, и их энергии отличаются на работу выхода электрона. Таким образом, электродные потенциалы металлов зависят не только от атомных свойств, но и от прочности связи атомов и электронов в простом веществе, от энергии сольватации. Если электрод инертный (не расходуется и не образуется, как Pt в водородном электроде), то его природа не влияет на равновесный потенциал, но влияет на скорость установления равновесия. Здесь электрод - катализатор. Поэтому часто вместо термина “электродный потенциал” употребляют “окислительно-восстановительный потенциал” или “редокс-потенциал”.
Похожие работы
... подкрепляет своим одобрением неправильный или не вполне точный ответ ученика. 1.2 Совершенствование школьного химического эксперимента при проблемном обучении 1.2.1 Принципы разработки методической системы и содержания опытов по химии в системе проблемного обучения Характерной особенностью развивающего обучения является широкое использование проблемного подхода, который включает создание ...
ависимо от способа получения и места нахождения. 2. Строение внешнего электронного уровня атома калия и кальция. 1 правило Клечковского. Строение внешнего электронного уровня атома скандия. 2правило Клечковского У атома аргона остаются незанятыми все орбитали 3d-подуровня. Однако у следующих за аргоном элементов – калия и кальция – заполнение 3-го электронного слоя временно прекращается, и ...
... разовая) – 0,01%. 4 Содержание Введение......................................................................................................................4 Глава 1. Межпредметные связи в курсе школьного предмета химии на примере углерода и его соединений.......................................................................5 1.1 Использование межпредметных связей для формирования у учащихся ...
... учреждение страны, а в ее задачи входило усовершенствование наук, просвещение, а также усовершенствование мануфактур, ремесел и фабрик. В то же время в начале XIX столетия, особенно после Отечественной войны 1812 г., в развитии химии в России появились новые черты. Смена мануфактурного производства фабрично-заводским выдвинула перед учеными множество практических задач, связанных с рациональной ...
0 комментариев