Навигация
Процесс алюминотермии выражается химическим уравнением
4. Процесс алюминотермии выражается химическим уравнением
8Al + 3 Fe3O4 = 4Al2O3 + 9Fe ΔH<0. Рассчитайте, сколько теплоты выделится при сгорании 1 кг термита.
5. Возможен ли обжиг колчедана массой 1т по следующему уравнению химической реакции 4FeS2 + 11O2 →2 Fe2O3 + 8SO2 ∆H<0
6. Вычислите тепловой эффект образования NH3 из простых веществ, при стандартном условии по тепловым эффектам реакции:
2H2 + O2 = 2H2O(ж) ΔН01 = -571, 68 кДж,
NH3 + 3O2 = 6H2O(ж) + 2N2 ΔН02 = -1530,28 кДж.
7. Стандартный тепловой эффект реакции сгорания этана равен -1560 кДж. Рассчитайте стандартную теплоту образования этана, если известно, что
ΔfН0298 (H2O)= -285,84 кДж/моль и ΔfН0298(СО2) = -396,3 кДж/моль.
8. Вычислите тепловой эффект реакции восстановления оксида железа водородом, пользуясь следующими данными.
FeO + CO = Fe + CO2 ΔН = -13,19 кДж
CO + 1/2O2 = CO2 ΔН = -283,2 кДж
2H2 + 1/2O2 = 2H2O(г) ΔН = -242 кДж
9. Протекание, какой из приведенных реакций восстановления оксида железа (III) наиболее вероятно при 298 К.
Fe2O3(k) + 3H2(г) = 2Fe(к) + 3H2O(к)
Fe2O3(k) + 3С(графит) = 2Fe(к) + 3СO(к)
Fe2O3(k) + 3СО(г) = 2Fe(к) + 3СО2(к)
10. В какой их перечисленных ниже реакций тепловой эффект ΔН0298 будет стандартной теплотой SO3(г)
а) S(г) + 3/2 O2 = SO3(г)
а) S(г) + 1/2 O2 = SO3(г)
а) S(к) + 3/2 O2 = SO3(г)
3.1.2 Химическое равновесие
При протекании химической реакции через некоторое время устанавливается равновесное состояние (химическое равновесие). Слово «равновесие» означает состояние, в котором сбалансированы все противоположно направленные на систему воздействия. Тело, находящееся в состоянии устойчивого равновесия, обнаруживает способность возвращаться в это состояние после какого-либо возмущающего воздействия.
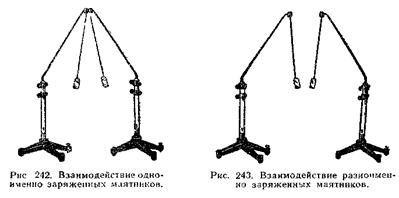
Примером тела, находящегося в состоянии устойчивого равновесия, может служить шарик, лежащий на дне ямки. Если его толкнуть в одну или другую сторону, он вскоре снова возвращается в состояние устойчивого равновесия. В отличие от этого шарик, лежащий на краю ямки, находится в состоянии неустойчивого равновесия — достаточно ничтожного толчка, чтобы он необратимо скатился в ямку.
Оба этих примера являются примерами статического равновесия. В химии, однако, приходится сталкиваться не столько со статическими равновесиями, столько с динамическими («подвижными»). Динамическое равновесие устанавливается, когда оказываются сбалансированными два обратимых или противоположных процесса. Динамические равновесия подразделяют на физические и химические. Наиболее важными типами физических равновесий являются фазовые равновесия. Система находится в состоянии химического равновесия, если скорость прямой реакции равна скорости обратной реакции.
Например, если скорость протекания реакции (константа скорости к1)
k1
А(г) + В(пар) ![]() АВ(г)
АВ(г)
равна скорости обратной реакции (константа скорости k2)
k2
АВ(г)![]() А(г) + В(пар)
А(г) + В(пар)
то система находится в динамическом равновесии. Подобные реакции называются обратимыми, а их уравнения записывают с помощью двойной стрелки:
k1
А(г) + В(пар) ![]() АВ(г)
АВ(г)
k2
Реакции, протекающие слева направо, называются прямой, справа налево – обратной.
Нужно подчеркнуть, что реакционная система остается в состоянии динамического равновесия лишь до тех пор, пока система остается изолированной. Изолированной называют такую систему, которая не обменивается с окружающей средой ни веществом, ни энергией.
Состояние химического равновесия обратимых процессов количественно характеризуется константой равновесия. Так, для обратимой реакции общего вида
k1
аA +bB ![]() сC + dD (1.2.1)
сC + dD (1.2.1)
k2
константа равновесия К, представляющая собой отношение констант скорости прямой и обратной реакций, запишется
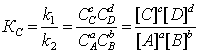 (1.2.2)
(1.2.2)
где, Кс– константа скорости реакции, зависящая от концентрации реагирующих компонентов; Сi или [ i ]- равновесная молярная концентрация i-того компонента;
a, b, c, d – стехиометрические коэффициенты веществ.
В правой части уравнения (1.2.2) стоят концентрации взаимодействующих частиц, которые устанавливают при равновесии, - равновесные концентрации.
Уравнение (1.2.2) представляет собой математическое выражение закона действующих масс при химическом равновесии. Для реакции с участием газов константа равновесия выражается через парциальные давления, а не через их равновесные концентрации. В этом случае константу равновесия обозначают символом Кр.
![]()
Рi- равновесные парциальные давления i-того компонента.
Сi - равновесная молярная концентрация компонентов.
a, b, c, d – стехиометрические коэффициенты веществ.
Состояние химического равновесия при неименных внешних условиях теоретически может сохраняться бесконечно долго. В реальной действительности, т.е. при изменении температуры, давления или концентрации реагентов, равновесии может «сместиться» в ту или иную сторону протекания процесса.
Изменения, происходящие в системе в результате внешних воздействий, определяется принципом подвижного равновесия – принципом Ле Шателье – Брауна. При воздействие на равновесную систему, любого внешнего фактора, равновесие в системе смещается в таком направлении, чтобы уменьшить воздействие этого фактора.
1. Влияние давления на равновесие химической реакции (для реакции, проходящей в газовой фазе).
aA + bB ![]() cC + dD
cC + dD
- если реакция идет с увеличением количества компонентов a + b < c + d, то повышение давления смещает равновесие химической реакции справа налево.
- если реакция идет с уменьшением количества компонентов a + b > c + d, при увеличении давления сдвиг равновесия произойдет слева направо.
- если количество компонентов одинаково a + b = c + d, то изменение давления не повлияет на положении равновесия.
2. Влияние инертного газа. Введение инертного газа подобно эффекту уменьшения давления (Ar, N2, водяной пар). Инертный газ не участвует в реакции.
3. Влияние изменения концентрации реагирующих веществ. При введение дополнительного количества вещества равновесие химической реакции сместиться в ту сторону где концентрация вещества уменьшается.
4. Влияние температуры на химическое равновесие реакции.
Если к равновесной системе подводится теплота, то в системе происходят изменения, чтобы ослабить это воздействие, т.е. процессы с поглощением теплоты. При экзотермических реакциях снижение температуру сместит равновесие слева направо, а при эндотермических реакциях повышение температуры сместит равновесие справа налево.
Зависимость Кр от температуры – уравнение Вант – Гоффа.
![]() ;
; ![]() ;
;
(![]() ); lnkT1 – lnkT2 =
); lnkT1 – lnkT2 = ![]()
Примеры решения задач
Похожие работы
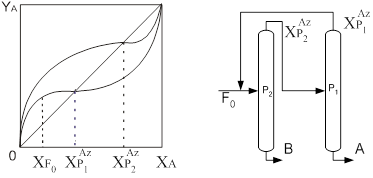
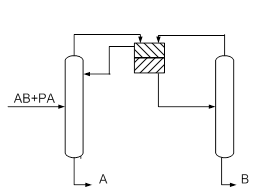
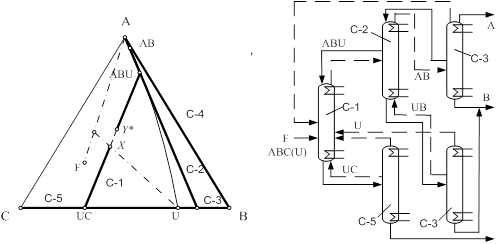
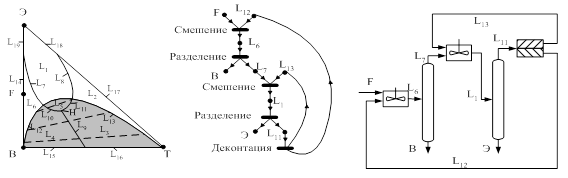
... принципа приближения и термодинамической обратимости к экстрактивной ректификации, с одной стороны, и выявить области оптимальности схем экстрактивной ректификации, с другой стороны. Постановка задачи Целью данной работы является разработка технологии разделения азеотропной смеси циклогексан – бензол – этилбензол методом экстрактивной ректификации, обладающей минимальными энергозатратами. Для ...
... , таблица). Метод моделирования позволяет активизировать познавательную деятельность учащихся на уроке. 2.2. Опытно – экспериментальная работа. Анализ ее результатов Изучив теоретические положения по использованию моделирования при решении задач в 5 классе, у автора возникло желание и интерес реализовать это на практике. Для того чтобы доказать или опровергнуть предположение, что ...
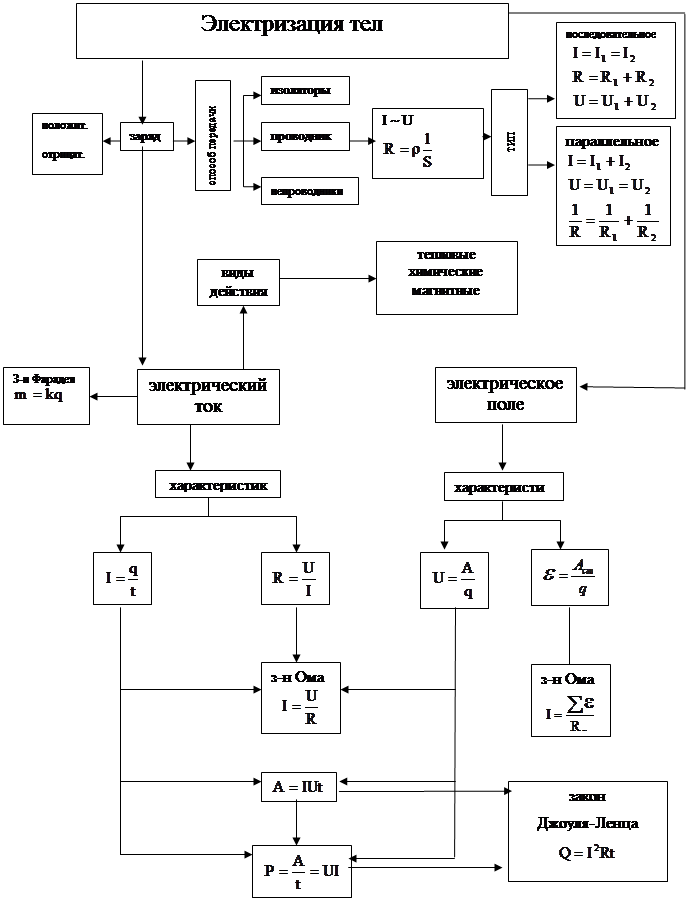
... и дидактические основы организации обучения позволяют более доступно объяснять изучаемый материал на уроках физики при изучении темы «Основы электродинамики». Анализ различных технологий позволил составить авторскую технологию развития у учащихся направленности на диалогическое общение при групповой форме обучения. От того, на сколько правильно будет построен процесс обучения при использовании ...
... групп – в виде краткого отчета о проделанной работе (демонстрация рисунков, таблиц). Далее идет обсуждение выступлений; учитель продумывает со своими коллегами трудовое задание [1]. 1.1 Межпредметные связи при решении расчетных задач К изучению математики учащиеся средней школы приступают на 7 лет раньше, чем к изучению химии. За этот период обучения они приобретают значительный объем ...
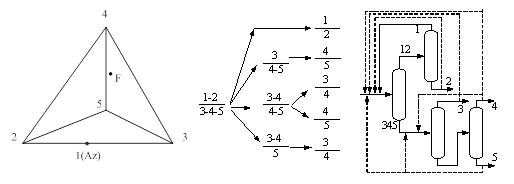

0 комментариев