Навигация
Реакция с дифениламином (фармакопейная)
1. Реакция с дифениламином (фармакопейная).
Реакцию проводят в концентрированной серной кислоте. Вначале происходит необратимое окисление дифениламина в дифенилбензидин:
2C6H5NHC6H5 — С6Н5 - NH - С6Н4 -С6Н4 - NH - С6Н5 + 2 Н+ + 2ё
дифениламин дифенилбензидин (бесцветный)
Две молекулы дифениламина отдают окислителю два электрона и теряют два иона водорода. Затем происходит обратимое окисление молекулы бензидина присутствующим окислителем до окрашенного в синий цвет дифенилдифенохинондиимина, при котором молекулы дифенилбензидина также отдает окислителю два электрона и теряет два иона водорода:
![]()
При стоянии синей смеси, ее окраска постепенно изменяется вначале на бурую, а затем - на желтую, вследствие необратимого разрушения синего продукта реакции.
Проведению реакции мешают как анионы - окислители (C103-,Br3, Cr207 и др.), так и анионы - восстановители (S2-, SO32-, S2O32-, 1- и др.).
Нитрат - ион NO3- дает аналогичную реакцию с дифениламином.
2. Реакция с сильными кислотами (фармакопейная).
NО2-+H+=HNO2
2HNO2 =N2O3 + Н20 — NO + NO2 + H2O (желто-бурые пары)
3.Реакция с иодидом калия (нитрит - ион - окислитель).
Нитрит - ион в кислой среде (НС1, H2SO4, CH3COOH) окисляет иодид - ионы до свободного иода:
2 N02- + 2 1- + 4 Н+ -> 12 + 2 N0 + 2 Н20
Образующийся йод обнаруживают реакцией с крахмалом (по посинению раствора) или экстрагируя его органическим растворителем - бензолом, хлороформом (органический слой окрашивается в фиолетовый цвет).
Нитрат - ион N03 не мешает проведению реакции, поэтому ионы N02- можно открыть в присутствии нитрат - ионов. Проведению реакции мешают окислители (МпО4-.Сг2О72- и др.).
4.Реакция с перманганатом калия (нитрит - ион - восстановитель).
5 N02- + 2 МпО4- + 6 Н+ — 5 N03- + 2 Мп2+ + 3 Н20
Проведению реакции мешают другие восстановители (S2-, SO32\ S2O32-, C2O42-, SCN\ АбОз3-,!-, Вг-), также реагирующие с МпО4- - ионами.
Нитрат - ион N03- не обесцвечивает раствор КМпО4 (отличие от нитрит - иона -фармакопейный тест). Розовый раствор перманганата калия обесцвечивается.
5.Реакция с реактивом Грисса - Илотвая.
Реактив Грисса - Илотвая - смесь сульфаниловой кислоты HSO3C6H4NIЬ с 1-нафтиламином C10P7NH2. Реакцию проводят в нейтральных или уксуснокислых растворах.Образующаяся в кислой среде в присутствии нитрит- иона азотистая кислота HN02 реагирует с сульфаниловой кислотой, давая соль диазония:
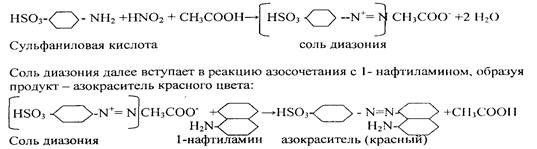
В результате раствор окрашивается в красный цвет.
Нитрат - ион NO3- аналогичной реакции не дает.
Вместо сульфаниловой кислоты используют и другие ароматические амины, а вместо 1-нафтиламина - 1 амино - 2- нафтол, 2- нафтол и т.д.
6. Реакция с солями аммония - реакция разложения (удаления) нитрит ионов.
N02 + NH4 = N2 + 2Н2О
Аналогична реакция с карбамидом:>
2N02 + 2 Н+ + СО (NH2)2 = 2 N2 + СО2 + 3Н2О
Эти реакции используют для удаления нитрит- ионов из раствора. Наблюдается выделение пузырьков газа - азота.
Чтобы убедиться в полноте протекания реакции, в пробирку прибавляют каплю раствора иодида калия KI и каплю крахмала. Если раствор не окрашивается в синий цвет, то это означает, что нитрит - ион в растворе отсутствует.
7. Реакция с антипирином (фармакопейная)
Реакцию проводят в слабокислой среде.
![]()
8. Другие реакции нитрит - иона.
Нитрит - ион с солями кобальта и KCI в уксуснокислой среде дает желтый кристаллический осадок гексанитрокобальтата (III) калия K3[Co(NO)2)6]; с FeSO4 в , сернокислой или уксуснокислой среде о.бразует комплекс состава [Fe(NO)SO4] бурого цвета и т.д.
Аналитические реакции нитрат - иона NO3-Нитрат - ион NO3- - анион одноосновной сильной азотной кислоты HNO3. В водных растворах бесцветный нитрат - ион не гидролизуется, обладает окислительными свойствами. Как лиганд NO3- - мало эффективен и образует неустойчивые нитракомплексы металлов. Нитраты металлов хорошо растворяются в воде.
В отличие от нитритов, нитраты не обесцвечивают подкисленные водные растворы перманганата калия (фармакопейный тест).
1.Реакция с дифениламином (фармакопейная).
Эта реакция - общая для NO3- и NO2- и проводится точно так же, как и для нитрит -иона (см. выше); только вместо раствора нитрита натрия используют раствор нитрата натрия или калия. Данной реакцией нельзя открывать нитраты в присутствии нитритов.
2.Реакция с металлической медью (фармакопейная).
Реакцию проводят в среде концентрированной H2SO4 при нагревании.
2 NO3- + 8 Н++ 3 Си = 3 Си2++ 2 NOT + 4 Н2О 2NO + О2 --> 2 NO2j'(жeлтo-бypыe пары)
3.Реакция с сульфатом железа (II) и концентрированной серной кислотой.
Реакцию проводят при нагревании:
3 Fe2+ + Nft- + 4 Н+ ->■ 3 Fe3++ NO + 2 Н2О Fe2++ NO + SO42- -> [Fe NO]SO4 (бурый)
Эту реакцию дает и нитрит - ион, поэтому нельзя открыть этой реакцией нитрат - ион в присутствии нитрит- иона. Проведению реакции мешают Вг-, Г, SO32-, S2O32', CrO42-, MnO42-.
4.Реакция с металлическим алюминием или цинком.
3 NO3- + 8 А1 + 5 ОН- + 18 Н2О -> 3 NH3 + 8 [Al (OH)4]-
Выделяющийся аммиак ощущается по запаху и окрашивает влажную красную лакмусовую бумагу в синий цвет.Проведению реакции мешают катионы аммония NH4+, выделяющие аммиак в щелочной среде, а также другие анионы, способные восстанавливаться до аммиака (NO2-, SCN-, ферро - и феррицианид — ионы).
5.Реакция с антипирином. Реакцию проводят в кислой среде.
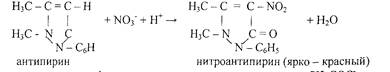
Ацетат - ион СН3СОО- - анион слабой одноосновной уксусной кислоты СН3СООН: в водных растворах бесцветен, подвергается гидролизу, не обладает окислительно -восстановительными свойствами; довольно эффективный лиганд и образует устойчивые ацетатные комплексы с катионами многих металлов. При реакциях со спиртами в кислой среде дает сложные эфиры.
Ацетаты аммония, щелочных и большинства других металлов хорошо растворяется в воде. Ацетаты серебра CH3COOAg и ртути (I) менее ацетатов других металлов растворимы в воде.
1.Реакция с хлоридом железа (III) (фармакопейная).
При рН = 5-8 ацетат - ион с катионами Fe(III) образует растворимый темно - красный (цвета крепкого .чая) ацетат или оксиацетат железа (III).
В водном растворе он частично гидролизуется; подкисление раствора минеральными кислотами подавляет гидролиз и приводит к исчезновению красной окраски раствора.
3 СНзСООН + Fe -->• (CH3COO)3Fe + 3 Н+
При кипячении из раствора выпадает красно-бурый осадок основного ацетата железа (III):
(CH3COO)3Fe + 2 Н2О <- Fe(OH)2 CH3COO + 2 СН3СООН
В зависимости от соотношений концентраций железа (III) и ацетат - ионов состав осадка может изменяться и отвечать, например, формулам: Fe ОН (СН3СОО)2, Fe3(OH)2O3 (CH3COO), Fe3 О (ОН)( СН3СОО)6 или Fe3(OH)2 (СН3СОО)7.
Проведению реакции мешают анионы СО32-, SO3'-, РО43-, [Fe(CN)6]4, образующие осадки с железом (III), а также анионы SCN- (дающие красные комплексы с катионами Fe3+), иодид - ион Г,окисляющийся до йода 12, придающего раствору желтую окраску.
2.Реакция с серной кислотой.
Ацетат - ион в сильно кислой среде переходит в слабую уксусную кислоту, пары которой имеют характерный запах уксуса:
СН3СОО- + Н+ <- СН3СООН
Проведению реакции мешают анионы NO2\ S2-, SO32-, S2O32-, также выделяющие в среде концентрированной H2SO4 газообразные продукты с характерным запахом.
3.Реакция образования уксусноэтилового эфира (фармакопейная).
Реакцию проводят в сернокислой среде. С этанолом:
СН3СОО- + Н+ -- СН3СООН СН3СООН + С2Н5ОН = СН3СООС2Н4 + Н2О
Выделяющийся этилацетат обнаруживают по характерному приятному запаху. Соли серебра катализируют эту реакцию, поэтому при ее проведении рекомендуется добавлять небольшое количество AgNO3.
Аналогично при реакции с амиловым спиртом С5НцОН образуется также обладающий приятным запахом амилацетат СН3СООС5Ни (-грушевая-) Ощущается характерный запах этилацетата, усиливающийся при осторожном нагревании смеси.
Аналитические реакции тартрат - иона РОС- СН(ОН) - СН(ОН) - СОСТ. Тартрат- ион - анион слабой двухосновной винной кислоты:
![]() НО-СН-СООН
НО-СН-СООН
НО -СН- СООН
Тартрат - ион хорошо растворим в воде. В водных растворах тартрат - ионы бесцветны, подвергаются гидролизу, склонны к комплексообразованию, давая устойчивые тартратные комплексы с катионами многих металлов. Винная кислота образует два ряда солей – средние тартраты, содержащие двух зараядный тартрат – ион СОСН(ОН)СН(ОН)СОО-, и кислые тартраты – гидротартраты, содержащие однозарядный гидротартрат – ион НОООСН(ОН)СН(ОН)СОО-. Гидротартрат калия (-винный камень-) КНС4Н4О6 практически не растворм в воде, что используется для открытия катионов калия. Средняя кальциевая соль также мало растворима в воде. Средняя калиевая соль К2С4Н4О6 хорошо растворяется в воде.
I. Реакция с хлоридом калия (фармакопейная).
С4Н4О62- + К++ Н+ -> КНС4Н4О61 (белый)
2. Реакция с резорцином в кислой среде (фармакопейная).
Тартраты при нагревании с резорцином мета - С6Н4(ОН)2 в среде концентрированной серной кислоты образуют продукты реакции вишнево - красного цвета.
3.Реакции с аммиачным комплексом серебра. Выпадает черный осадок металлического серебра.
4.Реакция с сульфатом железа (II) и пероксидом водорода.
Прибавление разбавленного водного раствора FeSO4 и Н2О2 к раствору, содержащему тартраты. приводит к образованию к образованию неустойчивого комплекса железа жатого цвета. Последующая обработка раствором щелочи NaOH приводит к кяншиовению комплекса голубого цвета.
Аналитические реакции цитрат - ионаЦитрат - ион -ООССН2 - С(ОН)(СОО-) - СН2СОО- - анион слабой трехосновной лимонной кислоты:

Лимонная кислота хорошо растворима в воде. В водных растворах цитрат - ионы бесцветны, подвергаются гидролизу, способны образовывать устойчивые цитратные комплексы с катионами многих металлов.
Средний нитрат натрия растворяется в воде. Средняя кальциевая соль лимонной свеклы мало растворима в горячей воде, но хорошо растворяется в холодной воде, что используется на практике. I. Реакция с хлоридом кальция (фармакопейная). Реакцию проводят в нейтральной среде при кипячении:
![]()
где Cit - - условное сокращенное обозначение среднего цитрат - иона. 2. Реакция образования пентабромацетона. Реакцию проводят в сернокислой среде.
Вначале в сернокислом растворе происходит окисление лимонной кислоты до апгтондикарбоновой кислоты О = С (CitCOOH)2:
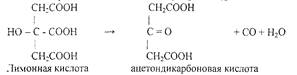
Затем ацетондикарбоновая кислота бромируется и переходит в пентабромацетон:
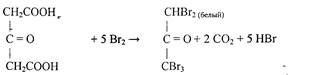
Проведению реакции мешают органические кислоты и фенолы, дающие осадки продуктов бромирования.
Похожие работы
... красного окрашивания раствора не наблюдаем, следовательно анион NO2-действительно в данной смеси отсутствует. Качественные реакции на анионы третьей аналитической группы Подтвердим присутствие в анализируемом веществе аниона NO3-. Проведем следующую реакцию: к нескольким каплям раствора неизвестного вещества прибавим 2-3 капли дефениламина и 5 капель концентрированной серной кислоты. Наблюдается ...
... состоит анализируемое вещество и какие ионы, группы атомов или молекулы входят в его состав. При исследовании состава неизвестного вещества качественный анализ всегда предшествует количественному, так как выбор метода количественного определения составных частей анализируемого вещества зависит от данных, полученных при его качественном анализе. Качественный химический анализ большей частью ...
... имеет свою специфику. Качественный химический анализ базируется на системе химических реакций, характерных для данного вещества - разделения, отделения и обнаружения. К химическим реакциям в качественном анализе предъявляют следующие требования. 1. Реакция должна протекать практически мгновенно. 2. Реакция должна быть необратимой. 3. Реакция должна сопровождаться внешним эффектом (АС): а) ...
... + 3H2SO4 = 2MnSO4 + K2SO4 + 5KNO3 + 3H2O Итак, существует большое число разновидностей количественного химического анализа, позволяющих определять разнообразные вещества в широких пределах концентраций. Среди химических методов анализа наиболее распространены титрометрические и гравиметрические методы. 9. Инструментальные методы анализа Инструментальные метода анализа обладают многими ...

0 комментариев