Навигация
Реакция с хинализарином
5. Реакция с хинализарином.
Реакцию проводят в щелочной среде. Образуется синий осадок комплексного соединения – хинализарината магния состава MgL(OH), где НL – условное обозначение молекулы хинализарина:
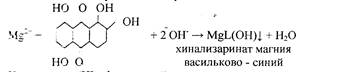
При небольшом содержании катионов Mg2+в растворе осадок не выпадает, а раствор окрашивается в цвет. Проведению реакций мешают катионы алюминия.
6. Реакция с растворимыми карбонатами (Nа2С03).
2 Mg2++ 2 Nа2С03 + Н2О = (МgОН)2С0з (белый аморфный) +4 Nа + СО2. Осадок (МgОН)2С0з,растворим в кислотах и в солях аммония.
7. Реакция с оксалатом аммония (NH4)С2О4.
Mg2++ (NH4)С2О4 = Mg С2О4 (белый) + 2 NH4
8. Катионы Mg2+ с дифенилкарбазидом (С6Н5 NHNH)2С0 образуют комплекс красно— фиолетового цвета.
Аналитические реакции катиона марганца
Аквокомплексы [Мn(Н2О)6]2+ марганца (II) окрашены в бледно — розовый цвет. Сильно разбавленные водные растворы солей марганца (и) практически бесцветны.
1. Реакции с щелочами и аммиаком: Мп2+ + 2 ОН- —+ Мп(ОН)2.
Белый осадок Мп(ОН)2 при стоянии темнеет за счет окисления кислородом воздуха вслелствие образования МпО(ОН)2: 2 Мп(ОН)2 + 02 = 2 МпО(ОН)2
В присутствии перекиси водорода: Мп2+ + 2 ОН + Н202 — МпО(ОН)2 + Н20 Осадок Мп(ОН)2 растворяется в разбавленных растворах сильных кислот и в насыщенном растворе хлорида аммония: Мп(ОН)2 + 2Н —+ Мп2+ +2 Н2О, Мп(ОН), 2NH4С1 — Мп +2 NН3Н2О + 2 С1
Осадок МпО(ОН)2 не растворяется при действии этих реагентов.
2. Реакция окисления катионов Мп2 до перманганат — ионов. Реации окисления проводят в отсутствие хлорид — ионов Сl, так как они восстанавливаются пермавганат — нонами до хлора Сl2:
2 МпО4 + 10 С2О8 + 16 Н — 2Мп2+ + 5 Сl2 + 8 Н20
а) Окисление висмугатом натрия в кислой среде.
2 Мп2+ + 5 NаВiО3 + 14 Н — 2 Мп04 + 5 Вi3 + 5Nа + 7 Н2О
Раствор окрашивается в малиново — фиолетовый цвет.
б). Окисление персульфатом аммония. Реакцию проводят в кислой среде в присутствии катализатора — солей серебра (Аg3) при нагревании:
2 Мп2 + 5 820i + 8 Н20 = 2 Мп04 + 10 $042 + 16 Н.
В горячем растворе возможно разложение перманганат— ионов, которое замедляется в присутствии фосфорной кислоты Н3РО4.
Раствор окрашивается в малиновый цвет.
в). Окисление диоксидом свинца в кислой среде при нагревании:
2 Мп2+ + 5 РЬО2 + 4 Н = 2МпО4 + РЬ2+ + 2 Н20
При избытке соли марганца (1I)образуется МпО(ОН)2. а не перманганат— ион.
З. Реакция с сульфид нонами: Мп2+ + S2-- — Мп S розовато-телесный Осалок Мп S растворяется в разбавленных кислотах.
Другие реакции марганца (II)
а) Катионы марганца образуют с аммиакатом серебра [Ag(NH3)2]+ смесь МпО(ОН)2 и металлического серебра буро-черного цвета:
Мп2+ + 2 [Ag(NH3)2]+ + 2 ОН- + 3 Н20 = МпО(ОН)2 + 2 Ag + 2 NH4 + 2NH3 Н20
б) карбонаты щелочных метталов аммония образуют с Мп2+ белый осадок МпСО3, растворимый в кислотах;
в) гидрофосфат натрия осаждает белый осадок Мп3(РО4)2; растворимый в минеральных и уксусной кислотах (отличие от Al3+, Cr3+, Fe3+).
Аналитические реакции катиона железа Fe2+
Акво-ионы железа (II) [Fe(H2O)6]2+ практически бесцветны, .поэтому растворы солей железа (II) обычно не окрашены.
1. Реакции с щелочами и аммиаком: Fei+ + 2 ОН- —- Fe(OH)?| (белый) На воздухе осадок постепенно темнеет: 4 Fe(OH)2 +О2 + 2 Н2О —> 4 Fe(OH)3| или с Н2О2.:2 Fe2+ + 4 ОН- + Н2О2 -> 2 Ре(ОН)3^(красно-бурый) Fe(OH)2 растворяется в кислотах, но не растворяется в щелочах.
2. Реакция с гексацианоферратом (III) калия - феррицианидом калия
(фармакопейная):Ре2+ + [Fe111 (CN)6f — Fe3+ + [Fe11 (CN)6]4-
4 Fe3+ + 3 [Fe (CN)6]4- + XH2O — Fe4[Fe (CN)6]3-XH2O
-турнбуллевая синь- (темно-синий)
Суммарно: 4Fe2+ +4[Fe-' (CN)6]3- + XH2O -♦ Fe111 [Fe- (CN)6]3-XH2O +[Fe- (CN)6]4-
Осадок не растворяется в кислотах, но разлагается в щелочной среде.
3.Реакция с сульфид - ионами (фармакопейная): Fe2+ + S2- —> FeSJ. (черный) Осадок растворяется в разбавленных минеральных кислотах и в уксусной кислоте.
4.Реакция с диметилглиоксимом (реактив Чугаева). Предел обнаружения 0,4 мкг.
(CH3CNOH)2 + Fe2+ + 2 NH4OH ->■ [Fe(C4H7N2O2)2] + NH3 + 2 H2O
реактив Чугаеварозово-красный комплекс
5.Окисление Fe2+ в FeJ+ растворами KMnO4, K2Cr207, HNO3
6.FeSO4 + 3 H2SO4 + 2 HNO3 = 3 Fe2(SO4)3 + 4 H2O + 2 NOT
До исчезновения бурой окраски, зависящей от образования нестойкого комплекса [Fe(NO)]SO4.
Аналитические реакции катионов железа (III) Fe3+
Акво-ионы железа (III) [Fe(H2O)6]3+ в водных растворах окрашены в желтый цвет и частично гидролизованы до растворимых гидроксоаквокомплексов [Fe(OH)n(H20)6.n]3--, также окрашенных в желто - бурый цвет. Поэтому водные растворы солей железа (III) имеют желтую или красновато-бурую окраску.
1.Реакция с щелочами и аммиаком: Fe3+ + 3 ОН' —> Fe(OH)3J. (красно - бурый) Осадок растворим в разбавленных кислотах: но не растворяется в насыщенном растворе NH4CI (в отличие от белого осадка Fe(OH)2), а также в растворах щелочей.
2.Реакция с гексацианоферратом (II) калия - с ферроцианидом калия
3.(фармакопейная).
Катионы Fe3+ при pH=2-3 реагируют с ферроцианидом калия:
4 Fe3+ + 3 [Fe (CN)6]4' + ХН2О — Fe4[Fe (CN)6]3-XH2O
-берлинская лазурь- (темно-синий)
Проведению реакции мешают окислители и восстановители. Окислители окисляют ферроцианид до феррицианида, а восстановители восстанавливают Fe(III) до Fe(II). Осадок не растворяется в кислотах, разлагается при прибавлении раствора щелочи: Fe4[Fe(CN)6]3 + 12 ОН- -> 4 Fe(OH)3 + 3 [Fe(CN)6]4-
3.Реакция с тиоционат — ионами при рН~3 (фармакопейная).
Для подавления образования гидроксокомплексов, содержащих ОН- группы, реакцию проводят в кислой среде. Раствор окрашивается в красный цвет.
[Fe(H2O)6]3+ + nNCS- = [Fe (NCS)n(H2O)6.J3-n + nH2O (где n=l,2,3,....6) Проведению реакции мешают: окислители, восстановители, ртуть(П)._фториды, тгодиды. фосфаты, цитраты, тартраты и др. Катионы Fe2+ не мешают. 4. Реакция с сульфосалициловой кислотой (фармакопейная).
FeJ+ образует с сульфосалициловой кислотой окрашенные комплексы. В зависимости от рН среды и соотношения реагирующих компонентов состав и окраска комплексов могут быть различными. Так, при рН=2-2,5 доминируют комплексы красного цвета, при рН=4-8 - бурого и при р№=9-11,5 - желтого. Наиболее устойчив комплекс желтого цвета (соотношение концентрации Fe(III) и сульфосалйциловой кислоты = 1:3): Fe +3 L2 '= [FeL3]3-
Где H2L - условное обозначение молекулы сульфосалициловой кислоты, a L- -обозначение сульфосалицилат-аниона, образовавшегося из сульфосалициловой кислоты, при отщеплении двух протонов:
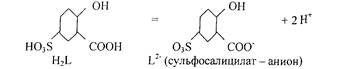
По-видимому, при рН=2-2,5 образующийся красный комплекс содержит железо (III) и Г2- в мольном соотношении 1:1, при рН=4 - 8 бурый комплекс - в мольном соотношении 1:2.
5.Реакция с сульфид - ионами (фармакопейная): 2 Fe3+ + 3 S2- -+ Fe2S3j (черный) Реакцию проводят в нейтральной или слабоаммиачной средах.
Осадок сульфида железа (III) растворяется в минеральных кислотах.
6.Гидрофосфат натрия Na2HPO4 образует с Fe3+ бледно-желтый осадок FePO4, растворимый в сильных кислотах, но нерастворимый в уксусной кислоте:
Fe3+ + 2 НРО42- = FePO4 + Н2РО4\
Карбонаты щелочных металлов и аммония-образуют бурый осадок основных солей, которые при кипячении превращаются в гидроокись.
7.Другие реакции Fe3+. Катионы Fe3+ при реакции с ферроном (7-иод-8-оксихинолин-5- еульфоновой кислотой) в кислой среде (р№=2,6) образуют комплексы зеленого цвета; при реакции с тайроном (1,2-диокси-3,5-дисульфобензолом) - комплексы синего цвета, изменяющие окраску на красную в щелочной среде; при реакции с купфероном красный осадок купфероната железа (III) и т.д.
Аналитические реакции сурьмы (III) и сурьмы (V) . Соли сурьмы гидролизуются в водных растворах с образованием осадков малорастворимых основных солей сурьмы. Соединения сурьмы окрашивают пламя газовой горелки в голубой цвет.
Аналитические реакции сурьмы (III)
1. Реакция с щелочами и аммиаком: [SbCl6]- + 5ОН- -> 8ЬО(ОН)3|(белый) + 6СГ + Н2О
Осадок растворяется в избытке щелочи: SbO(OH)3 + NaOH + H2O — Na[Sb(OH)6],
а также в сильных кислотах: SbO(OH)3 +6 НС1 -- H[SbCl6] + 4Н2О
2. Реакция гидролиза: [SbCl] + 2Н2О = Sb О2Cl (белый) + 4Н+ + 5 Cl-
Процесс называется реакцией образования красного осадка -сурьмяной киновари-. Мешает висмут (III), образующий черный осадок.
3. Реакция с сульфид ионами. Реакция проводится в кислой среде:
2 [SbCL6]-+ 2 S2O32- + 3 H2O = Sb2OS2С1 (красный) + 2 SO42- + 8 СI- + 6 H+. –
Осадок растворяется в избытке S2': Sb2S3 + 3 S2- —>2 SbS33',
в концентрированной НС1 при нагревании: Sb2S3 +8 НС1 —+ 2 H[SbCl4] + 3 H2S, в растворах щелочей: Sb2S3 +4 NaOH --■ Na[Sb(OH)4] + Na3SbS3
5.Реакции восстановления сурьмы (III) до сурьмы (0) в кислой среде:
[SbCL,]- + А1° -> Sb° + А13+ + 4 СГ; 2 [SbCl4]- + 3 Zn° - 2 Sb° + 3 Zn2+ + 8 СГ
6.Другие реакции сурьмы (IIII). При взаимодействии сурьмы (III) с фосфорно-молибденовой гетерополикислотой образуется продукт реакции синего цвета - -молибденовая синь-, экстрагируемый амиловым спиртом. С метилфлуороном
С13Н4О2(ОН)3СН3 сурьма (III) в присутствии Н2О2 и НС1 дает продукт красного цвета (капельная реакция на фильтровальной бумаге). Такие окислители, как КМпО4, К2Сг207, КВгО3 и другие, окисляют в растворах сурьму (III) до сурьмы (V).
Аналитические реакции висмутаСоли висмута (III) гидролизуются в водных растворах с образованием осадков малорастворимых оксосоединений – солей висмутила, формально содержащих катион висмутила BiO+ (напрмер BiOС1, BiONО3).
1. Реакция с щелочами и аммиаком: (BiС16)3- + 3 ОН- = Bi (ОН) 3 (белый) + 6 С1-
Осадок расворяется в минеральных кислотах. При нагревании желтеет вследствие образования оксогидроксида висмута (III): Bi (ОН) 3 = Bi ОН + Н2О
4.Реакция гидролиза: (BiС16)3- + Н5О = Bi ОС1 (белый) + 2 НС1 + 3 С1-
Осадок не растворяется в растворах винной кислоты и ее солей.
Похожие работы
... красного окрашивания раствора не наблюдаем, следовательно анион NO2-действительно в данной смеси отсутствует. Качественные реакции на анионы третьей аналитической группы Подтвердим присутствие в анализируемом веществе аниона NO3-. Проведем следующую реакцию: к нескольким каплям раствора неизвестного вещества прибавим 2-3 капли дефениламина и 5 капель концентрированной серной кислоты. Наблюдается ...
... состоит анализируемое вещество и какие ионы, группы атомов или молекулы входят в его состав. При исследовании состава неизвестного вещества качественный анализ всегда предшествует количественному, так как выбор метода количественного определения составных частей анализируемого вещества зависит от данных, полученных при его качественном анализе. Качественный химический анализ большей частью ...
... имеет свою специфику. Качественный химический анализ базируется на системе химических реакций, характерных для данного вещества - разделения, отделения и обнаружения. К химическим реакциям в качественном анализе предъявляют следующие требования. 1. Реакция должна протекать практически мгновенно. 2. Реакция должна быть необратимой. 3. Реакция должна сопровождаться внешним эффектом (АС): а) ...
... + 3H2SO4 = 2MnSO4 + K2SO4 + 5KNO3 + 3H2O Итак, существует большое число разновидностей количественного химического анализа, позволяющих определять разнообразные вещества в широких пределах концентраций. Среди химических методов анализа наиболее распространены титрометрические и гравиметрические методы. 9. Инструментальные методы анализа Инструментальные метода анализа обладают многими ...

0 комментариев